Rivestimento in carbonio drogato F Anodo Nano-Si ad alta capacità: preparazione mediante fluorurazione gassosa e Prestazioni per lo stoccaggio del litio
Autore: SU Nan, QIU Jieshan, WANG Zhiyu. Drogato F Anodo Nano-Si rivestito di carbonio ad alta capacità: preparazione mediante fluorurazione gassosa e prestazioni per lo stoccaggio del litio. Giornale dei materiali inorganici, 2023, 38(8): 947-953 DOI:10.15541/jim20230009
Astratto
Gli anodi di Si hanno un immenso potenziale nello sviluppo di ioni di litio ad alta energia batterie. Ma il rapido fallimento dovuto all’enorme cambiamento di volume legato all’assorbimento del Li ostacola la loro applicazione. Questo lavoro riporta una fluorurazione di gas facile ma poco tossica modo per produrre materiali anodici nano-Si rivestiti con carbonio drogato con F. Rivestimento di il nano-Si con carbonio drogato con F contenente difetti elevati può proteggere efficacemente il Si dall'enorme cambiamento di volume sullo stoccaggio del Li, facilitando al tempo stesso il trasporto del Li+ e formazione di un'interfase elettrolitica solida ricca di LiF (SEI) stabile. Questo anodo mostra capacità elevate di 1540-580 mAh·g-1 in vari tassi attuali di 0,2-5,0 A·g-1, pur mantenendo 75% di capacità dopo 200 cicli. Questo metodo affronta anche i problemi di costo elevato e tossicità delle tradizionali tecniche di fluorurazione che utilizzano il fluoro fonti come XeF2 e F2.
Parole chiaveï¼ Batteria agli ioni di litio; Anodo Si; Carbonio drogato F; fluorurazione gassosa metodo
Sviluppare un efficiente stoccaggio dell’energia e le tecnologie di conversione contribuiranno a raggiungere l’obiettivo del “carbon peaking”. neutralità del carbonioâ. Le batterie agli ioni di litio sono attualmente una delle più diffuse hanno utilizzato tecnologie di stoccaggio dell’energia ad alta efficienza [1]. Commerciale, però gli anodi di grafite hanno una bassa capacità di stoccaggio del litio, che limita notevolmente la capacità di stoccaggio del litio densità energetica delle batterie agli ioni di litio [2]. Il silicio presenta i vantaggi di basso riserve potenziali e abbondanti e la sua capacità specifica teorica (4200 mAh·g-1) è molto più alto di quello dell'anodo di grafite, quindi è considerato a materiale anodico candidato per sostituire la grafite [3]. I materiali in silicio raggiungono stoccaggio del litio basato sulla reazione di lega reversibile con ioni di litio, ma questo processo è accompagnato da enormi variazioni di volume (~400%), che portano a spolveramento rapido e guasto dell'elettrodo, che diventano un collo di bottiglia fondamentale limitare l'applicazione pratica degli anodi di silicio [3-4].
Negli ultimi anni, i ricercatori hanno sviluppato una varietà di strategie per migliorare la stabilità ed elettrochimica prestazioni degli anodi di silicio. Come: nanometrizzazione [5], strutturale composito con carbonio conduttivo e altri materiali [6-7], ecc. Migliorare il stabilità strutturale dell'anodo di silicio alleviando lo stress meccanico associato all’espansione del volume dello stoccaggio del litio a livello microscopico scala. Sviluppare nuovi elettroliti o additivi elettrolitici per migliorare la stabilità ed efficienza coulombiana della fase di interfaccia dell'elettrolita solido (SEI) sulla superficie dell'anodo di silicio [8]. Sviluppare polimeri efficienti leganti (come sodio carbossimetilcellulosa, sodio alginato, poliacrilico polirotassano a base acida [9], ecc.). Rafforzare la forza di legame tra attivi materiali, tra materiali attivi e rete conduttiva e tra pellicola dell'elettrodo e collettore di corrente [9-10]. Tra questi, il rivestimento in carbonio è uno dei mezzi più efficaci per migliorare la stabilità strutturale degli anodi di silicio e modulare le proprietà della superficie e dell'interfaccia [3-4,11]. Tuttavia, strettamente Lo strato di carbonio rivestito altamente stabile ostacola anche il trasporto e i limiti degli ioni di litio la piena prestazione dell'anodo di silicio.
Inoltre, il volume ripetuto cambiamenti dell'anodo di silicio durante il processo continuo di carica e scarica causano inoltre la rottura e la crescita continua della pellicola SEI, con conseguente la continua perdita di litio attivo ed elettrolita sulla superficie dell'elettrodo [12]. In risposta ai problemi di cui sopra, questo studio propone un efficiente metodo di fluorurazione in fase gassosa per rivestire la superficie del materiale dell'anodo di silicio con uno strato di carbonio amorfo altamente difettoso ricco di elementi di fluoro migliorarne la struttura e la stabilità dell'interfaccia. Rispetto al tradizionale tecnologia di fluorurazione che utilizza fonti di fluoro ad alto costo e altamente tossiche come XeF2 o F2 [13], questa strategia è più semplice e meno tossica. IL Lo strato di carbonio drogato con fluoro che riveste la superficie dei materiali in nano-silicio può tamponano efficacemente l'espansione del volume degli anodi di silicio incorporati al litio migliorando al contempo le capacità di trasporto degli ioni di litio. E un SEI altamente stabile film ricco di fluoruro inorganico è costruito in situ per raggiungere l'obiettivo di migliorare la stabilità del ciclo dell'anodo di silicio.
1 Metodo sperimentale
1.1 Preparazione del materiale
Preparazione del rivestimento in carbonio nano-silicio (Si@C):0,3 g di nanosilice commerciale la polvere (dimensione delle particelle 20~100 nm, reagente di Aladino) è stata sottoposta ad ultrasuoni disperso in 28 mL di un solvente misto di acqua deionizzata ed etanolo (volume rapporto 5:2). Dopo aver aggiunto 0,4 ml di 3-amminopropiltrietossisilano, agitare per 2 ore per formare una dispersione uniforme A. Sciogliere 0,115 g di 4,4-diidrossidifenile solfuro e 0,1 g di 3-amminofenolo in 28 mL di un solvente misto di deionizzato acqua ed etanolo (rapporto in volume 5:2) per formare una soluzione omogenea B. Miscelare dispersione A e soluzione B in modo uniforme, aggiungere 0,1 ml di acqua ammoniacale, agitare per 30 minuti, quindi aggiungere 0,14 ml di soluzione di formaldeide (37%~40%) e reagire con la costante agitazione a 30 °C per 12 h. Dopo la reazione, la resina fenolica è rivestita la nanosilice (Si@AF) è stata ottenuta mediante centrifugazione e lavaggio con etanolo e acqua deionizzata alternativamente per tre volte. È stato calcinato in gas argon a 800 °C per 3 ore per ottenere nano-silicio rivestito di carbonio (Si@C).
Preparazione di drogati con fluoro nanosilicio rivestito di carbonio (Si@C-F): 100 mg Si@C e 200 mg il fluoruro di polivinilidene (PVDF) è stato posto in un forno tubolare protetto da argon. La barca al quarzo contenente PVDF si trova a monte del flusso d'aria e il la barca al quarzo contenente Si@C è situata a valle del flusso d'aria. È arrostito a 600 °C per 3 ore per ottenere nano-silicio rivestito di carbonio drogato con fluoro (Si@C-F).
1.2 Assemblaggio della batteria e test delle prestazioni elettrochimiche
1.2.1 Assemblaggio batteria
Assemblare la batteria a bottone CR2016 per i test. Mescolare il materiale attivo, il nerofumo conduttivo e legante sodico carbossimetilcellulosa in modo uniforme in un rapporto di massa di 7:2:1. Deionizzato è stata aggiunta acqua come solvente e disperdente e la sospensione ottenuta è stata uniformemente rivestito sul foglio di rame come elettrodo di lavoro. La materia attiva il carico era di 0,8~1,0 mg·cm-2. Come contatore sono stati utilizzati fogli di metallo al litio elettrodi ed elettrodi di riferimento. L'elettrolita è una soluzione DOL/DME disciolto in 1,0 mol/L di LiTFSI (litio bistrifluorometansolfonato immide) e 2,0% LiNO3(DOL è 1,3-diossolano, DME è glicole etilenico dimetil etere, volume rapporto 1:1). Assemblare la cella in un vano portaoggetti riempito di argon (contenuto di acqua < 0,1 μL/L, contenuto di ossigeno < 0,1 μL/L).
1.2.2 Test delle prestazioni della batteria
Utilizzare l'IVIUM Vertex.C.EIS elettrochimico workstation per analizzare il meccanismo di reazione e la cinetica di reazione del batteria utilizzando il metodo della Voltammetria Ciclica (CV). L'intervallo di tensione è 0,01~1,5 V e la velocità di scansione è 0,05~0,5 mV·s- 1. Impedenza elettrochimica La spettroscopia (EIS) è stata utilizzata per analizzare la dinamica degli elettrodi. La frequenza del test l'intervallo era di 100 kHz~10 mHz e l'ampiezza della tensione di disturbo era di 5,0 mV. Il tester per batterie Land CT2001A è stato utilizzato per studiare le prestazioni di accumulo del litio utilizzando il metodo di carica e scarica a corrente costante. La finestra di tensione era 0,01~1,5 V (rispetto a Li/Li+) e la densità di corrente era 0,2~5,0 A·g-1.
2 Risultati e discussione
2.1 Analisi dell'aspetto, della struttura e della composizione dei materiali
Il processo di preparazione di I materiali nano-silicio rivestiti con carbonio drogato con fluoro sono mostrati nella Figura 1. Innanzitutto, vengono preparate nanoparticelle di silicio rivestite con polimero (Si@AF). Reazione di polimerizzazione di condensazione fenolo-aldeide e convertita in nanoparticelle di nano-silicio amorfo rivestite di carbonio (Si@C) ad alta temperatura. Poi come fonte di fluoro viene utilizzato il fluoruro di polivinilidene e il fluoro è drogato nello strato di carbonio esterno alle nanoparticelle di silicio attraverso la fase gassosa metodo di fluorurazione ad alta temperatura. La Figura 2 (a) mostra i modelli XRD di Materiali Si@C e Si@C-F. Picchi di diffrazione situati a 2θ=28°, 47°, 56°, 69° e 76°. Corrispondono al cristallo (111), (220), (311), (400) e (331) piani di silicio monocristallino (JCPDS 77-2108) rispettivamente. L'ampio picco situato a 2θ=25°~26° è attribuita alla struttura di carbonio ordinata a corto raggio formata dalla carbonizzazione del prodotto di polimerizzazione per condensazione fenolica. IL strato di rivestimento in carbonio ad alta conduttività ed eccellente flessibilità strutturale può alleviare efficacemente il fallimento della polverizzazione dei materiali siliconici durante il processo di carica e scarica e migliora la conduttività dell'elettrodo. La Figura 2(b) è lo spettro Raman dei materiali Si@C e Si@C-F, con ovvio picchi di assorbimento che compaiono a 515, 947, 1350 e 1594 cm-1. Tra questi, il i picchi di assorbimento a 515 e 947 cm-1 sono i picchi caratteristici di silicio cristallino, che derivano dal fotofonone del primo ordine scattering e scattering trasversale dei fotofononi del secondo ordine del silicio rispettivamente [14]. I picchi di assorbimento a 1350 e 1594 cm-1 corrispondono a configurazione del carbonio aromatico che allunga la vibrazione (modalità G) e il disordinato struttura del carbonio difettosa (modalità D), rispettivamente. In generale, il il rapporto di intensità della modalità D e della modalità G (ID/IG) può essere utilizzato per misurare il grado di difetti e disordini dei materiali in carbonio [15]. Rispetto al materiale Si@C (ID/IG=0,99), l'ID/IG del materiale Si@C-F aumenta a 1,08. Ciò dimostra che il il processo di fluorurazione può aumentare i difetti dello strato di rivestimento in carbonio, che è vantaggioso per rivestire saldamente il nano-silicio migliorando al tempo stesso gli ioni di litio capacità di trasporto.
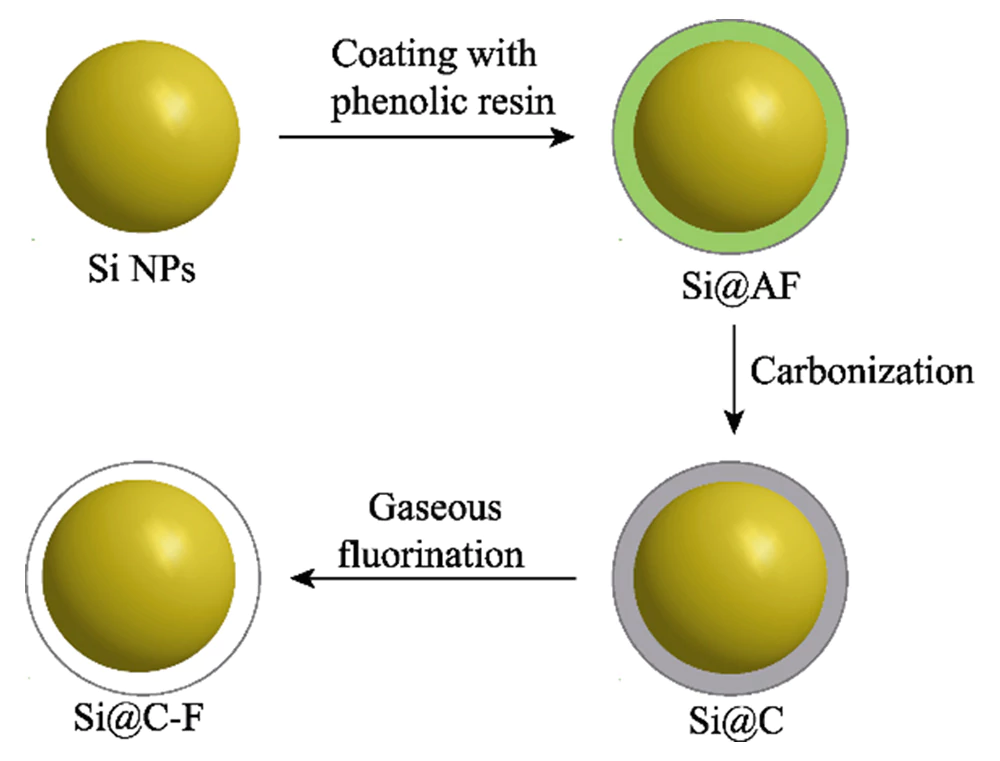
Fig. 1 Illustrazione schematica della produzione di Si@C-F
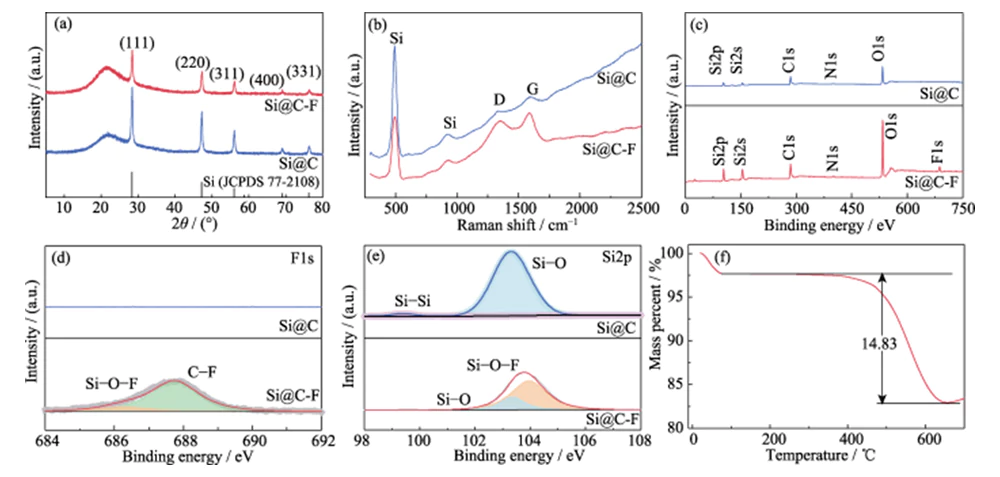
Fig. 2 (a) modelli XRD, (b) spettri Raman, (c) XPS scansione di rilevamento, (d) F1 ad alta risoluzione e (e) spettri Si2p XPS di Si@C e Si@C-F, (f) curva TGA di Si@C-F
Lo spettro completo dell'XPS mostra che Il materiale Si@C contiene elementi O, N, C e Si (Figura 2 (c)). L'atomico frazione di elemento F nel materiale Si@C-F ottenuto dopo fluorurazione il trattamento è di circa l’1,8%. Nello spettro XPS F1 ad alta risoluzione (Figura 2 (d)), i due picchi caratteristici all'energia di legame di 686,3 e 687,8 eV corrispondono rispettivamente a CF e Si-O-F e CF è il dominante uno. Mostra che il trattamento di fluorurazione ha introdotto con successo il fluoro elemento nello strato di carbonio amorfo rivestito sulla superficie del nano-silicio. IL Gli spettri XPS Si2p ad alta risoluzione (Figura 2 (e)) e F1s dimostrano che gli atomi di Si interagiscono chimicamente con l'elemento F nello strato di carbonio formando Si-O-F legami, il che è vantaggioso per il rivestimento stretto dello strato di carbonio sul superficie in silicio. L'analisi termogravimetrica (TGA) mostra che la frazione di massa di Si nel materiale Si@C-F è pari a circa l'85,17% (Figura 2(f)).
L'analisi SEM mostra che il Si@C-F il materiale è composto da nanoparticelle con una dimensione <100 nm (Figura 3 (a~c)). Dopo la carbonizzazione ad alta temperatura e il trattamento di fluorurazione in fase gassosa, il materiale di carbonio è ancora uniformemente rivestito sulla superficie delle nanoparticelle di silicio.
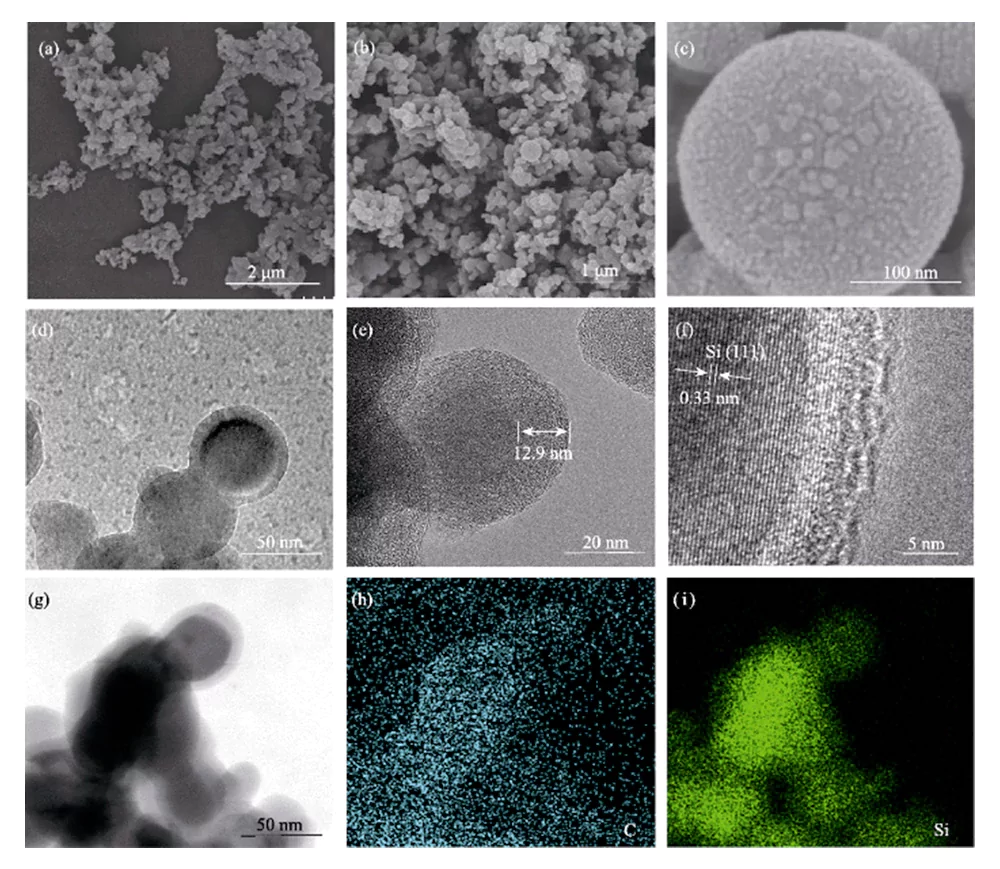
Fig. 3 (a-c) immagini SEM, (d-f) immagini TEM e (g-i) mappatura elementare di Si@C-F
L'analisi TEM mostra che il silicio le nanoparticelle sono completamente e uniformemente rivestite in uno strato di carbonio con a spessore di circa dieci nanometri, formando una struttura nucleo-guscio (Figura 3(d~e)). Le nanoparticelle di silicio hanno una struttura monocristallina, in cui il la spaziatura del reticolo di 0,328 nm corrisponde al piano cristallino (111) del Si, e lo strato di carbonio drogato con fluoro che lo ricopre ha una struttura amorfa (Figura 3(f)). Lo spettro di distribuzione degli elementi dimostra che gli elementi C e Si lo sono distribuito uniformemente in Si@C-F (Figura 3(g~i)).
2.2 Proprietà elettrochimiche di materiali
La Figura 4(a, b) è la curva CV dei materiali anodici Si@C e Si@C-F. La velocità di scansione è 0,1 mV·s-1 e l'intervallo di tensione è 0,01~1,5 V. Nel primo ciclo, il picco ampio e debole nell'intervallo 0,1~0,4 V corrisponde a processo irreversibile di decomposizione dell'elettrolita per formare un film SEI; IL il picco di riduzione a 0,01 V corrisponde al processo del silicio cristallino formando una lega di silicio-litio (LixSi) attraverso la reazione di lega. Durante il successivo processo di carica, i due picchi di ossidazione a 0,32 e 0,49 V corrispondono al processo di deallegazione di LixSi per formare silicio amorfo [16]. Fluorurazione il trattamento può ottenere effetti di drogaggio e incisione strutturale. Un gran numero di difetti strutturali vengono introdotti nello strato di carbonio amorfo rivestito sul superficie del materiale Si per formare un trasporto tridimensionale di ioni di litio canale, accelerare il trasporto degli ioni di litio e migliorare l'elettrochimica reattività del materiale Si. Pertanto, Si@C-F presenta una nitidezza maggiore Picco di ossidazione delitiazione a 0,49 V rispetto all'anodo Si@C senza fluoro doping. Durante il successivo processo di scarico, il nuovo picco di riduzione a 0,19 V corrisponde al processo di inserimento del litio nel silicio amorfo formato durante il primo processo di ricarica [16-17]. All’aumentare del numero di cicli, le posizioni del picco di ossidazione e del picco di riduzione nella curva CV n cambiamento più lungo, indicando che i materiali anodici Si@C e Si@C-F seguono un percorso simile meccanismo di accumulo del litio in lega dopo la prima carica e scarica. Durante questo processo, il picco di ossidazione e il picco di riduzione sono gradualmente aumentati, che riflette un tipico processo di attivazione dell'elettrodo.
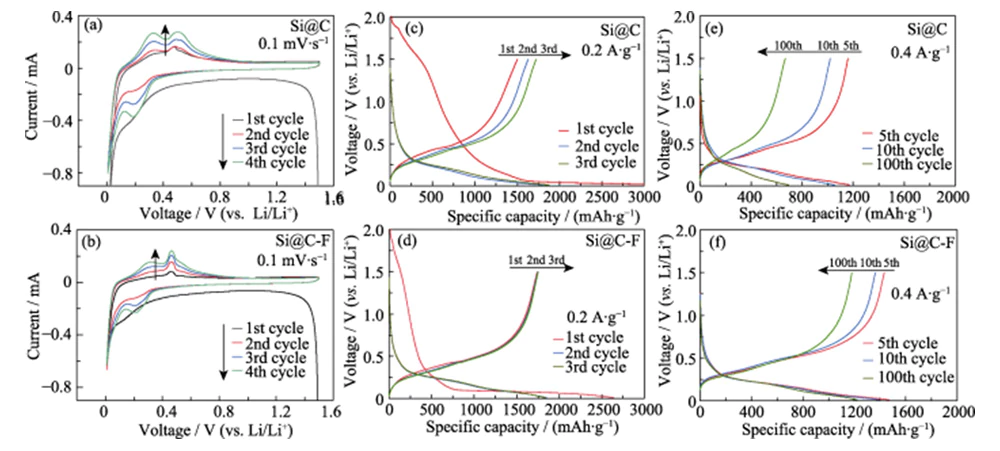
Fig. 4 (a, b) curve CV a una velocità di scansione di 0,1 mV·s-1 e curve di tensione di carica-scarica a (c, d) 0,2 e (e, f) 0,4 A·g-1 per (a, c, e) Anodi Si@C e (b, d, f) Si@C-F
Nella carica corrente costante e test di scarica, il materiale dell'anodo di Si è stato sottoposto a ciclo e attivato 4 volte a densità di corrente inferiore (0,2 A·g-1), quindi la sua stabilità del ciclo è stata testata a a densità di corrente di 0,4 A·g-1. La Figura 4 (c, d) mostra la carica galvanostatica e curve di scarica degli anodi Si@C e Si@C-F a 0,2 A·g-1 e la tensione è 0,01~1,5 V. Durante il primo processo di scarica, entrambi formavano un lungo piattaforma nell'intervallo di tensione < 0,1 V, corrispondente al processo di inserimento del litio nella lega di silicio cristallino. Questo processo è spesso accompagnato da una bassa efficienza prima Coulombiana. Durante il primo processo di carica, la lega silicio-litio viene delitiata e trasformata in silicio amorfo con un'energia di attivazione inferiore per l'inserimento del litio [18], facendo aumentare il potenziale di inserimento del litio a 0,1~0,3 V dopo la prima carica e scarica. Rispetto al Si@C, la capacità specifica della prima scarica (2640 mAh·g-1) dell'anodo Si@C-F è leggermente inferiore. Tuttavia, la capacità specifica della prima carica (1739,6 mAh·g-1) è maggiore e la prima efficienza Coulombiana (65,9%) è superiore di circa il 45,8% rispetto a quella dell'anodo Si@C. La curva carica-scarica della regione SEI dell'elettrodo negativo Si@C-F è più corta di quella di Si@C, indicando che sulla superficie si forma una pellicola SEI più stabile. Questo perché lo strato di carbonio drogato con fluoro favorisce la formazione di un film SEI contenente componenti inorganici (come LiF) e una maggiore stabilità sulla superficie dell'anodo di silicio, riducendo così la perdita irreversibile di litio e il consumo di elettrolita [19].
La Figura 4(e~f) mostra le curve di carica e scarica di Si@C e Elettrodi negativi Si@C-F con una densità di corrente di 0,4 A·g-1 dopo l'attivazione. Dopo 100 cicli l'anodo Si@C-F può ancora mantenere un'elevata capacità specifica di 1223 mAh·g-1, con un tasso di ritenzione della capacità 85% (Figura 5(a)). Sotto nelle stesse condizioni, la capacità dell'elettrodo negativo Si@C senza il trattamento di fluorurazione si deteriora rapidamente durante il processo di carica e scarica, e il tasso di mantenimento della capacità dopo 100 cicli era solo del 62%. Lo dimostra lo strato di rivestimento in carbonio drogato con fluoro ha un effetto significativo sul miglioramento la stabilità del ciclo dell'anodo di silicio. Commerciale gli anodi in nano-silicio senza rivestimento in carbonio si guastano dopo più di 10 cicli a causa dell'enorme espansione del volume e dello spolveramento strutturale durante il deintercalazione del litio. Durante questo processo, la capacità specifica di Gli elettrodi negativi Si@C-F e Si@C aumentano gradualmente nei primi 10-20 cicli dovuti all'effetto di attivazione. Con una densità di corrente elevata pari a 0,2~5,0 A·g-1, l'anodo Si@C-F può mantenere un'elevata capacità specifica di 1540~580 mAh·g-1, mostrando un'eccellente ritenzione di capacità (Figura 5(b)). Ad alta corrente densità di 5,0 A·g-1, il suo tasso di ritenzione della capacità è superiore di circa il 78%. di quello di Si@C. Quando la densità di corrente viene ulteriormente ridotta a 0,2 A·g-1, la capacità specifica può essere ripristinata a 1450 mAh·g-1, indicando che è la struttura è altamente stabile durante lo stoccaggio del litio ad alta velocità. Dopo 200 cicli di carica-scarica con una densità di corrente di 0,2 A·g-1, l'anodo Si@C-F può mantenere una capacità specifica 75%. Il tasso di mantenimento della capacità del L'anodo Si@C senza trattamento di fluorurazione è solo del 40% (Figura 5 (c)). Questo anodo mostra anche prestazioni di stoccaggio del litio migliori rispetto al materiale dell'anodo di silicio riportato in letteratura (Tabella 1).
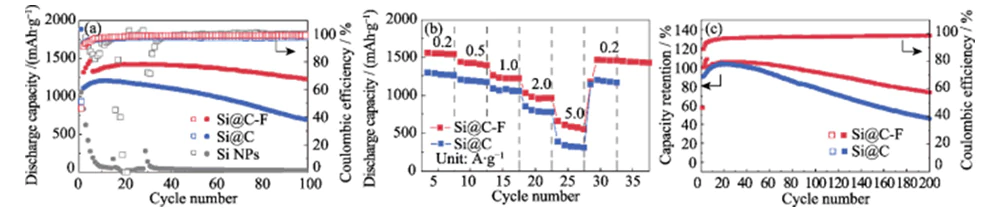
Fig. 5 (a) Stabilità del ciclismo con una densità di corrente di 0,4 A·g-1 con anodi attivati da 4 cicli a 0,2 A·g-1 prima del ciclo e (b) capacità di velocità a varie densità di corrente compreso tra 0,2 e 5,0 A·gâ1 e (c) mantenimento della capacità con una densità di corrente di 0,2 A·g-1 per lo stoccaggio del litio nell'anodo Si@C e Si@C-F
Tabella 1 Confronto tra l'anodo Si@C-F e riportato anodo a base di Si nelle prestazioni elettrochimiche
|
Materiali |
CE iniziale |
Capacità iniziale/(mAh·g-1) |
Ritenzione della capacitàritenzione |
Rif. |
|
Si@C-F |
65,9% |
2640 |
85% (100 cicli) |
Questo lavoro |
|
nano-Si/TiN@ |
71% |
2716 |
59,4% (110 cicli) |
<[20] |
|
Si@C@RGO |
74,5% |
1474 |
48,9% (40 cicli) |
[21] |
|
Si@FA |
65% |
1334 |
68,7% (100 cicli) |
[22] |
|
p-Si@C |
58% |
3460 |
57,5% (100 cicli) |
[23] |
|
Si@vuoto@C |
- |
900 |
70% (100 cicli) |
[24] |
|
Si/C@C |
- |
1120 |
80% (100 cicli) |
[25] |
Ad alta corrente densità di 5,0 A·g-1, il suo tasso di ritenzione della capacità è superiore di circa il 78%. di quello di Si@C. Quando la densità di corrente viene ulteriormente ridotta a 0,2 A·g-1, la capacità specifica può essere ripristinata a 1450 mAh·g-1, indicando che è la struttura è altamente stabile durante lo stoccaggio del litio ad alta velocità. Dopo 200 cicli di carica-scarica con una densità di corrente di 0,2 A·g-1, l'anodo Si@C-F può mantenere una capacità specifica 75%. Il tasso di mantenimento della capacità del L'anodo Si@C senza trattamento di fluorurazione è solo del 40% (Figura 5 (c)). Questo anodo mostra anche prestazioni di stoccaggio del litio migliori rispetto al materiale dell'anodo di silicio riportati in letteratura (Tabella 1). La quantità di drogaggio di fluoro nel rivestimento Lo strato di carbonio ha un impatto significativo sulle prestazioni di stoccaggio del litio Anodo Si@C-F. Quando la quantità di drogaggio del fluoro è inferiore all'1,8% di frazione atomica, la stabilità del ciclo dell'anodo Si@C-F migliora significativamente man mano che la quantità di drogaggio del fluoro aumenta (Figura 6). Ciò è dovuto all'effetto potenziato del drogaggio del fluoro sulle proprietà di trasporto degli ioni di litio del carbonio strato di rivestimento e stabilità del film SEI sulla superficie del silicio materiale. Quando il rapporto di drogaggio del fluoro è troppo elevato (2,7%), il rivestito in carbonioIl materiale dell'anodo di Si mantiene ancora una buona stabilità del ciclo, ma il la capacità specifica diminuisce significativamente. Ciò è dovuto alla perdita di Si attivo causato dall'attacco di specie di fluoro in fase gassosa durante l'alta temperatura fluorurazione. Quando la quantità di drogaggio del fluoro è pari all'1,8 percento atomico, il Si@C-F l'anodo mostra una stabilità del ciclo ottimale e un'elevata capacità specifica.
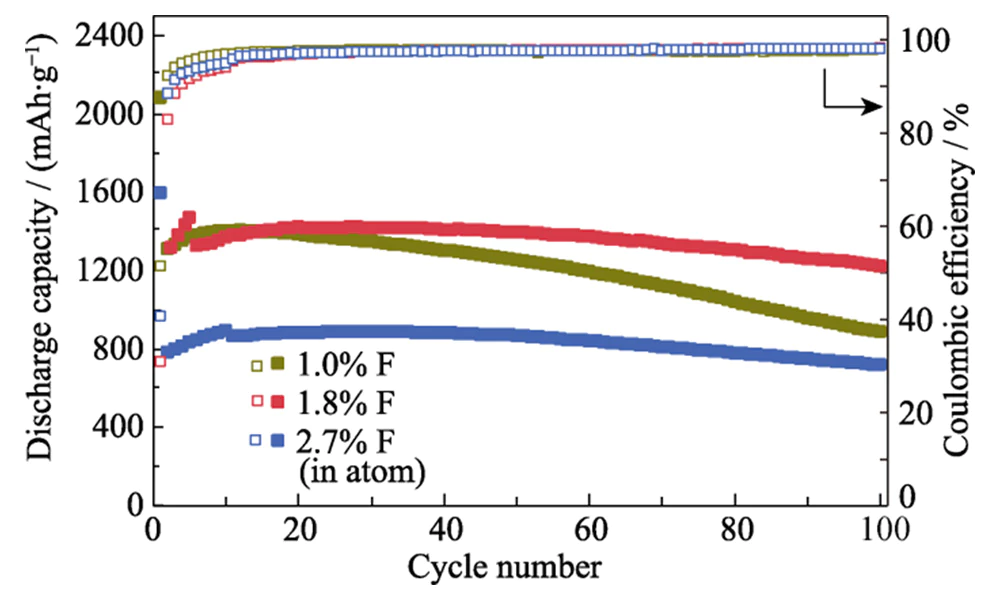
Fig. 6 Stabilità ciclica degli anodi Si@C-F con diversi Rapporti F con una densità di corrente di 0,4 A·g-1 con anodi attivati da 4-10 cicli a 0,2 A·g-1 prima del ciclo
Gli spettri EIS di Si@C e Si@C-F gli anodi sono costituiti da curve a semiarco nella regione delle frequenze medio-alte e linee rette inclinate nella regione delle basse frequenze (Figura 7 (a)). Il semiarco La curva nella gamma delle frequenze medio-alte è correlata al trasferimento di carica resistenza (Rct) e la linea retta inclinata nella gamma delle basse frequenze riflette principalmente l'impedenza di Warburg (ZW) della diffusione degli ioni di litio [26]. Prima di caricare e scaricare, il Rct degli elettrodi negativi Si@C-F e Si@C sono simili, ma il primo ha uno ZW inferiore a causa dell'elevata difettosità strato di carbonio drogato con fluoro che ricopre la superficie. Dopo la carica e la scarica cicli, l'Rct (5,51 Ω) dell'anodo Si@C-F è significativamente inferiore a quello dell'anodo Si@C (21,97 Ω) (Figura 7(b)), e la ZW è molto inferiore alla più recente. Ciò dimostra che il film di interfaccia SEI ricco di fluoro indotto dal Lo strato di carbonio drogato con fluoro può migliorare efficacemente la carica dell'interfaccia e capacità di trasporto degli ioni di litio.
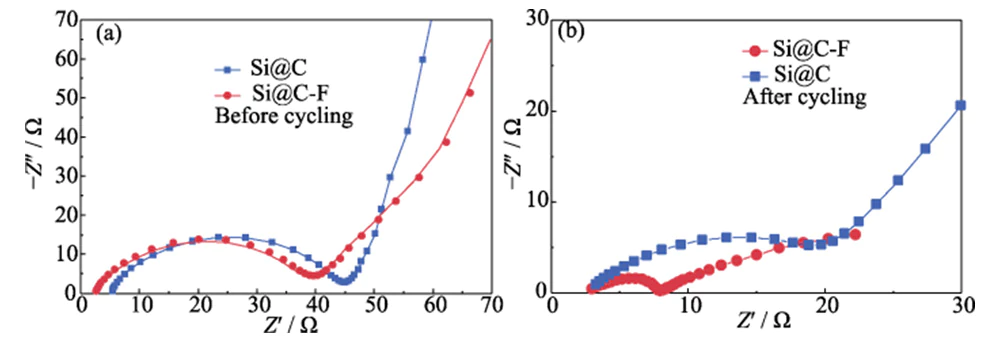
Fig. 7 Grafici di Nyquist degli anodi Si@C e Si@C-F (a) prima e (b) dopo il ciclo ad una densità di corrente di 0,4 A·g-1
2.3 Caratterizzazione della struttura dell'elettrodo dopo carica e scarica
Caratterizzazione al SEM dopo carica e scarica cicli (Figura 8(a~c)) mostra che ciò è dovuto alla significativa espansione del volume effetto del silicio durante il processo di inserimento del litio, lo spessore del L'elettrodo Si@C è aumentato del 132,3%. Ciò non solo ostacola la trasmissione di ioni ed elettroni, aumenta la resistenza interna e la polarizzazione del elettrodo, ma provoca anche un enorme stress meccanico, causando la rottura dell'elettrodo rottura e separazione dal collettore corrente, causando la prestazione del L'anodo Si@C decade rapidamente (Figura 5 (c)). In confronto, l'elettrodo lo spessore dell'anodo Si@C-F è aumentato solo del 26,6% dopo la carica e cicli di scarica e mantenuto una buona stabilità strutturale dell'elettrodo (Figura 8(d~f)). Ciò dimostra che lo strato di carbonio drogato con fluoro introdotto può tamponano efficacemente l'effetto di espansione del volume dell'inserimento del litio nel silicio materiali su scala micro, migliorando così la stabilità strutturale del elettrodo su scala macro dal basso verso l'alto.
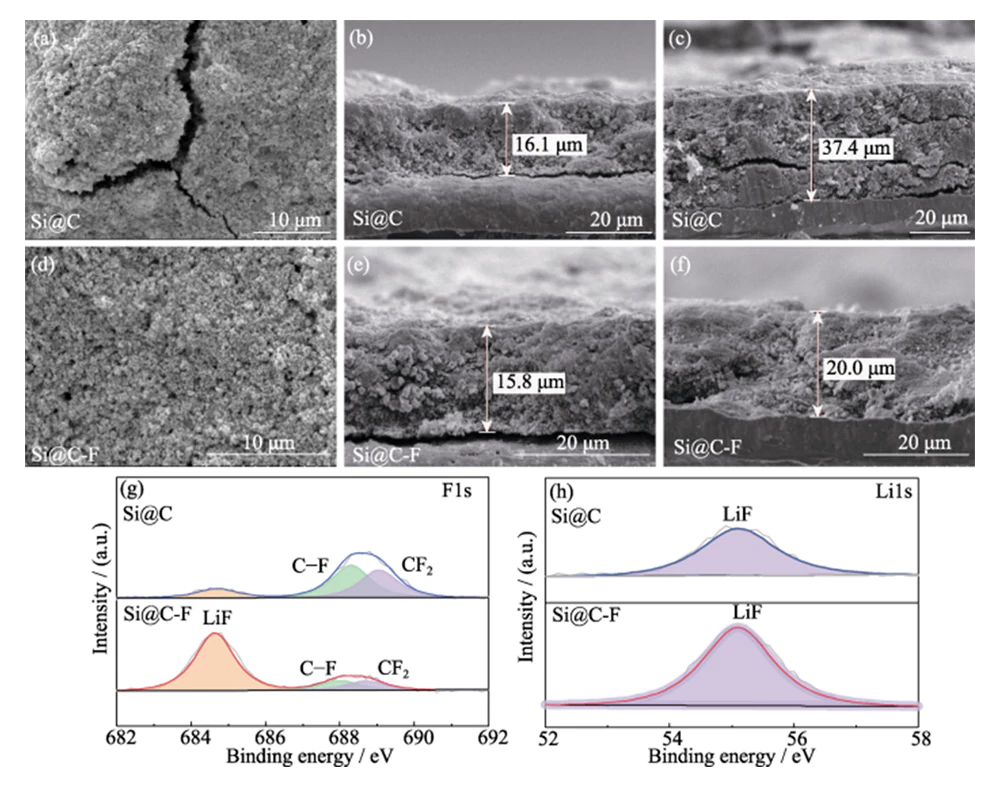
Fig. 8 Immagini SEM superiori degli anodi (a) Si@C e (d) Si@C-F dopo il ciclismo; Immagini SEM in sezione trasversale degli anodi Si@C (b, c) e Si@C-F (e, f) (b, e) prima e (c, f) dopo il ciclismo; Ad alta risoluzione (g) F1 e (h) Li1 Spettri XPS di SEI su anodi Si@C e Si@C-F dopo il ciclo
La composizione del film SEI sulla superficie di Si@C e gli elettrodi negativi Si@C-F dopo i cicli di carica e scarica sono stati analizzati mediante XPS (Figura 8(g~h)). Nello spettro XPS F1 ad alta risoluzione, l'attacco corrispondono picchi di energia alle energie di legame di 684,8, 688,3 e 689,1 eV rispettivamente a LiF, obbligazioni CF e CF2. Di conseguenza, ci sono anche picchi caratteristici corrispondenti alle specie LiF nei Li1 ad alta risoluzione Spettro XPS, che indica che si forma un film SEI contenente specie LiF la superficie dell'anodo di silicio. Rispetto all'anodo Si@C, il contenuto di LiF sulla superficie dell'anodo Si@C-F è più alto, indicando che il LiF nell'anodo La pellicola SEI non deriva solo dalla decomposizione dei sali di litio nel elettrolita, ma anche dalla F nello strato di carbonio drogato con fluoro. IL la formazione di LiF ad alto modulo può aumentare efficacemente la resistenza strutturale del film SEI e inibiscono la variazione di volume dell'inserimento di litio nel silicio materiali. Allo stesso tempo, l'ampio gap di banda e le proprietà isolanti del LiF può ridurre lo spessore del SEI e ridurre la perdita irreversibile iniziale di litio. La lega LixSi, il prodotto di litiazione di LiF e Si, ha un'elevata interfaccia energia e può adattarsi meglio alla deformazione plastica del silicio litiato anodo durante il ciclismo, migliorando così ulteriormente la stabilità del ciclismo elettrodo [19].
3 Conclusione
In questo studio, drogato con fluoro I materiali in nano-silicio rivestiti di carbonio sono stati preparati attraverso un metodo semplice e metodo di fluorurazione in fase gassosa a bassa tossicità. La ricerca mostra che il doping con fluoro (1,8% F), da un lato, aumenta i difetti dello strato di rivestimento in carbonio la superficie del silicio e fornisce abbondanti canali di trasporto degli ioni di litio mentre riveste strettamente il nano-silicio per sopprimerne l'espansione del volume. Dall'altro D'altra parte, sulla superficie del materiale viene indotto un film SEI altamente stabile ricco di LiF materiale nano-silicio, migliorando ulteriormente la stabilità e l'efficienza coulombiana dell'anodo di silicio. Grazie a ciò, la prima efficienza coulombiana del Anodo di nano-silicio rivestito di carbonio drogato con fluoro migliorato al 65,9%. Ad una corrente densità di 0,2~5,0 A·g-1, presenta un'elevata capacità specifica di 1540~580 mAh·g-1 e può mantenere 75% della capacità iniziale dopo 200 cicli. Questo lavoro fornisce nuove idee per la progettazione e la costruzione dell'anodo di silicio materiali con elevata capacità ed elevata stabilità.
Riferimento
[1] NIU S S, WANG Z Y, YU M L, et al.Basato su MXene elettrodo con pseudocapacità e capacità volumetrica migliorate per l'alimentazione tipo e stoccaggio al litio a lunghissima durata.ACS Nano, 2018, 12(4): 3928.
[2] SU X, WU Q L, LI J C et al. Nanomateriali a base di silicio per batterie agli ioni di litio: una recensione.Advanced Energy Materials, 2014, 4(1): 1300882.
[3] GE M Z, CAO C Y, GILL M B et al. Progressi recenti negli elettrodi a base di silicio: dalla ricerca fondamentale alla pratica applicazioni.Materiali avanzati, 2021, 33(16): 2004577.
[4] LI P, ZHAO G Q, ZHENG X B, et al. Recenti progressi sui prodotti a base di silicio materiali anodici per applicazioni pratiche con batterie agli ioni di litio.Energia Materiali di archiviazione, 2018, 15: 422.
[5] LIU X H, ZHONG L, HUANG S, et al. Dipende dalla dimensione frattura delle nanoparticelle di silicio durante la litiazione.ACS Nano, 2012, 6(2): 1522.
[6] LUO W, WANG Y X, CHOU S L, et al. Spessore critico dei composti fenolici strato interfacciale di carbonio a base di resina per migliorare la stabilità del ciclo lungo anodi di nanoparticelle di silicio.Nano Energy, 2016, 27: 255.
[7] DOU F, SHI L Y, CHEN G R, materiali anodici compositi in silicone/carbonio per batterie agli ioni di litio.Recensioni sull'energia elettrochimica, 2019, 2(1): 149.
[8] JIA H P, ZOU LF, GAO P Y, et al. Ad alte prestazioni Anodi di silicio abilitati da ininfiammabili localizzati ad alta concentrazione elettroliti.Advanced Energy Materials, 2019, 9(31): 1900784.
[9] CHOI S H, KWON T W, COSKUN A, et al. Altamente elastico leganti integranti polirotassani per anodi di microparticelle di silicio in litio batterie agli ioni.Science, 2017, 357: 279.
[10] LI Z H, ZHANG Y P, LIU T F, et al. Anodo di silicio con elevata efficienza coulombiana iniziale mediante legante trifunzionale modulato per batterie agli ioni di litio ad alta capacità. Energia avanzata Materiali, 2020, 10(20): 1903110.
[11] XU Z L, CAO K, ABOUALI S, et al.Studio dei meccanismi di litiazione del Si rivestito con carbonio ad alte prestazioni anodi mediante microscopia in situ. Materiali per l'immagazzinamento dell'energia, 2016, 3: 45.
[12] TEKI R, MONI K D, RAHUL K, et al. Anodi di silicio nanostrutturati per batterie ricaricabili agli ioni di litio.Piccola, 2009, 5(20): 2236.
[13] XIA S X, ZHANG X, LUO L L, et al. Altamente stabile e anodo metallico al litio ad altissima velocità abilitato da fibre di carbonio fluorurate. Small, 2021, 17: 2006002.
[14] ZHANG S L, WANG X, HO K S, et al. Spettri Raman in a regione ad ampia frequenza del silicio poroso di tipo p.Journal of Applied Fisica, 1994, 76(5): 3016.
[15] HUANG W, WANG Y, LUO G H, et al.99,9% Nanotubi di carbonio a pareti multiple di purezza mediante vuoto ricottura ad alta temperatura. Carbonio, 2003, 41(13): 2585.
[16] MCDOWELL M T, LEE S W, NIX W D et al. 25° anniversario articolo: comprendere la litiazione del silicio e di altri anodi leganti per batterie agli ioni di litio. Advanced Materials, 2013, 25(36): 4966.
[17] CHIAVE SI, MORCRETTE M, TARASCON J Analisi della funzione di distribuzione M.Pair e studi NMR allo stato solido del silicio elettrodi per batterie agli ioni di litio: comprendere la (de)litiazione meccanismi.Journal of American Chemical Society, 2011, 133(3): 503.
[18] GAO H, XIAO L S, PLUMEL I, et al. Reazioni parassitarie in dimensioni nanometriche anodi di silicio per batterie agli ioni di litio. Nano Letters, 2017, 17(3): 1512.
[19] CHEN J, FAN X L, LI Q et al. Progettazione di elettroliti ricchi di LiF interfacce elettrolita solido per consentire anodi in lega microdimensionata ad alte prestazioni per batterie.Nature Energy, 2020, 5(5): 386.
[20] ZHANG P, GAO Y Q, RU Q et al. Preparazione scalabile di materiali porosi Anodo in nano-silicio/TiN@carbonio per batterie agli ioni di litio. Superficie applicata Scienza, 2019, 498: 143829.
[21] SU M R, WAN H F, LIU Y J, et al. Multistrato Composito a base di Si rivestito di carbonio come anodo per batterie agli ioni di litio. Polvere Tecnologia, 2018, 323: 294.
[22] PUJ B, QIN J, WANG Y Z, et al.Sintesi della struttura della micro-nanosfera composito silicio-carbonio come materiale anodico per batterie agli ioni di litio. Prodotto chimico Lettere di fisica, 2022, 806: 140006.
[23] GAO R S, TANG J, YU X L, et al. Un silicio-carbonio simile a un sandwich composito preparato mediante polimerizzazione superficiale per un rapido stoccaggio di ioni di litio.
Nanoenergia, 2020, 70: 104444.
[24] GONG X H, ZHENG Y B, ZHENG J, et al. Tuorlo-guscio compositi silicio/carbonio preparati da una lega di alluminio-silicio come anodo materiali per batterie agli ioni di litio.Ionics, 2021, 27: 1939.
[25] LIA Y R, WANG R Y, ZHANG J W, et al.Sandwich struttura di anodi in nanofibra di silicio/carbonio rivestiti di carbonio per ioni di litio batterie.Ceramics International, 2019, 45: 16195.
[26] YANG X M E ROGACH A L.Tecniche elettrochimiche nella ricerca sulle batterie: un tutorial per non elettrochimici. Advanced Energy Materials, 2019, 9(25): 1900747.