Categorie
nuovo blog
- Confronto tra i materiali catodici delle batterie: NMC vs LFP vs NCA
- Tendenze nella produzione di batterie agli ioni di litio nel 2026: una guida per gli acquirenti B2B.
- Guida dettagliata al processo di produzione delle batterie agli ioni di litio
- Principali cause di perdite nella sigillatura delle celle della tasca
- Formazione e classificazione nella produzione di batterie agli ioni di litio
Tag
Elettrolita a film sottile LiSiON amorfo per batterie al litio a film sottile completamente allo stato solido
Autore: XIA Qiuying, SUN Shuo, ZAN Feng, XU Jing, XIA Hui
Scuola dei Materiali Scienza e ingegneria, Università di scienza e tecnologia di Nanchino, Nanchino 210094, Cina
Astratto
La batteria al litio a film sottile (TFLB) completamente allo stato solido è considerata l'ideale fonte di energia per dispositivi microelettronici. Tuttavia, lo ionico relativamente basso la conduttività dell'elettrolita amorfo allo stato solido limita il miglioramento di prestazioni elettrochimiche per TFLB. In questo lavoro, litio-silicio amorfo I film sottili di ossinitruro (LiSiON) vengono preparati mediante sputtering con magnetron come elettrolita allo stato solido per TFLB. Con condizioni di deposizione ottimizzate, il Il film sottile LiSiON mostra un'elevata conduttività ionica di 6,3×10-6 Sâcm-1 a temperatura ambiente temperatura e un'ampia finestra di tensione superiore a 5 V, che lo rendono un film sottile adatto elettrolita per TFLB. Un TFLB MoO3/LiSiON/Li lo è costruito sulla base dell'elettrolita a film sottile LiSiON con grandi specifiche capacità (282 mAhâg-1 a 50 mAâg-1), buona velocità capacità (50 mAhâg-1 a 800 mAâg-1) e accettabile ciclo di vita (ritenzione della capacità del 78,1% dopo 200 cicli), dimostrando la fattibilità di questo elettrolita per applicazioni pratiche.
Parole chiaveï¼ LiSiON; pellicola sottile elettrolita; batteria al litio interamente allo stato solido; batteria a film sottile
Il rapido sviluppo dell'industria microelettronica, come ad esempio sistemi microelettromeccanici (MEMS), microsensori, schede intelligenti e micro dispositivi medici impiantabili, porta ad una crescente domanda di dispositivi integrati accumulo di energia di dimensioni micro[1,2]. Tra le tecnologie delle batterie disponibili, la batteria al litio a film sottile completamente allo stato solido (TFLB) è considerata l'ideale fonte di alimentazione per dispositivi microelettronici grazie alla loro elevata sicurezza, dimensioni ridotte, design power-on-chip, lunga durata e basso tasso di autoscarica. Come uno di i componenti chiave di TFLB, l'elettrolita a film sottile allo stato solido, svolge un ruolo vitale ruolo nel determinare le proprietà del TFLB[3]. Perciò, lo sviluppo di un elettrolita a film sottile allo stato solido ad alte prestazioni è sempre una cosa importante traguardo importante per lo sviluppo del TFLB. Attualmente il più utilizzato L'elettrolita nel TFLB è l'ossinitruro di litio-fosforo amorfo (LiPON), che ha una conduttività ionica moderata (2×10-6 Sâcm-1), bassa conduttività elettronica (~10-14 Sâcm-1), ampio voltaggio finestra (~5,5 V) e buona stabilità di contatto con il litio[4,5]. Tuttavia, è la conduttività ionica è relativamente bassa, il che impedisce il futuro sviluppo di TFLB ad alta potenza per la prossima era dell'Internet delle cose (IoT)[6]. Così è urgente sviluppare nuovi elettroliti a film sottile con maggiore conduttività ionica, così come un'ampia finestra di tensione e una buona stabilità del contatto con il litio TFLB di prossima generazione.
Tra i vari materiali elettrolitici inorganici allo stato solido, il solido Li2O-SiO2 il sistema di soluzione e le loro fasi deuterogene sono stati identificati come potenzialmente sottili elettroliti a film grazie alla loro rapida conduzione tridimensionale del litio canali[7]. Ad esempio, Chen, et al.[8] riportato che l'elettrolita solido Li4.4Al0.4Si0.6O4-0.3Li2O sostituito con Al ha un'elevata conduttività ionica di 5,4Ã10-3 Sâcm-1 a 200 â. Adnan, et al.[9] ha scoperto che il composto Li4Sn0.02Si0.98O4 possiede un valore massimo di conduttività di 3,07×10-5 Sâcm-1 a temperatura ambiente. Tuttavia, i lavori precedenti sui sistemi elettrolitici Li2O-SiO2 si concentravano principalmente sulla polvere materiali con elevata cristallinità, mentre è stato riportato un lavoro molto limitato le loro controparti amorfe a film sottile per TFLB. Poiché TFLB è in genere costruito depositando sottili pellicole di catodo, elettrolita e strato di anodo strato, il film elettrolitico deve essere preparato a temperatura relativamente bassa per evitare le interazioni sfavorevoli tra catodo ed elettrolita, che provocano la rottura e il cortocircuito del TFLB[1,2]. Così, sviluppo di un elettrolita Li2O-SiO2 con caratteristica amorfa preparato a bassa temperatura la temperatura è importante per TFLB. Sebbene lavori recenti[6] mostrino che un'elevata conduttività ionica del litio di 2,06×10-5 Sâcm-1 può essere ottenuta mediante Li-Si-P-O-N amorfo film sottile, la sua stabilità di contatto con gli elettrodi ed elettrochimica la stabilità in TFLB deve ancora essere studiata. Pertanto, è critico importante sviluppare un elettrolita a film sottile a base di Li2O-SiO2 ad alte prestazioni e dimostrare la sua effettiva applicazione in TFLB.
In questo lavoro è stato utilizzato un film sottile di ossinitruro di litio e silicio amorfo (LiSiON). preparato mediante sputtering di magnetron a radiofrequenza (RF) a temperatura ambiente e studiato come elettrolita a stato solido per TFLB. Il potere di sputtering e il il flusso del gas di lavoro N2/Ar è stato ottimizzato per ottenere le migliori condizioni di deposizione per il film sottile LiSiON. Inoltre, per dimostrare l'applicabilità dell'art ottimizzato per l'elettrolita LiSiON per TFLB, è stata costruita una cella completa MoO3/LiSiON/Li e la sua le prestazioni elettrochimiche sono state sistematicamente studiate.
1 sperimentale
1.1 Preparazione di film sottili LiSiON
I film sottili di LiSiON sono stati preparati mediante sputtering con magnetron RF (Kurt J. Lesker) utilizzando un target Li2SiO3 (76,2 mm di diametro) a temperatura ambiente per 12 ore Prima della deposizione, la pressione della camera era ridotta a meno di 1×10-5 Pa. La distanza dal bersaglio al substrato era di 10 cm. I campioni depositati sotto una potenza RF di 80, 100 e 120 W al flusso di 90 sccm N2 sono contrassegnati rispettivamente come campione LiSiON-80N9, LiSiON-100N9 e LiSiON-120N9. E i campioni depositati sotto una potenza RF di 100 W al flusso di 90 sccm N2 e 10 sccm Ar, 90 sccm N2 e 50 sccm Ar, 50 sccm N2 e 50 sccm Ar sono contrassegnati come campione LiSiON-100N9A1, LiSiON-100N9A5 e LiSiON-100N5A5, rispettivamente.
La pellicola di MoO3 è stata preparata mediante magnetron reattivo a corrente continua (CC). sputtering (Kurt J. Lesker) utilizzando un bersaglio al Mo di metallo puro (76,2 mm di diametro) secondo il nostro precedente rapporto[10]. La distanza dal bersaglio al substrato era di 10 cm e DC la potenza di sputtering era di 60 W. La deposizione è stata eseguita sul substrato temperatura di 100 â per 4 h al flusso di 40 sccm Ar e 10 sccm O2, seguito da un trattamento di ricottura in situ a 450 â per 1 ora. LiSiON-100N9A1 è stato quindi depositato sul film MoO3 come elettrolita. Successivamente è stata creata una pellicola di litio metallico di circa 2 μm di spessore depositato sul film LiSiON mediante evaporazione termica sotto vuoto (Kurt J. Lesker). La fase finale di fabbricazione prevedeva la deposizione del collettore di corrente Cu e il processo di incapsulamento.
Le strutture cristalline di i campioni sono stati caratterizzati mediante diffrazione di raggi X (XRD, Bruker D8 Advance). Le morfologie e le microstrutture dei campioni sono state caratterizzate per campo microscopio elettronico a scansione ad emissione (FESEM, FEI Quanta 250F) dotato di spettroscopia a raggi X a dispersione di energia (EDS). Le composizioni elementari del i campioni sono stati analizzati mediante spettrometria di massa al plasma accoppiato induttivamente (ICP-MS, Agilent 7700X). La composizione chimica e le informazioni sul legame dei campioni sono stati misurati mediante spettroscopia fotoelettronica a raggi X (XPS, Escalab 250XI, Thermo Scientifico).
1.4 Misure elettrochimiche
È stata misurata la conduttività ionica dell'elettrolita a film sottile LiSiON utilizzando una struttura a sandwich di Pt/LiSiON/Pt. L'impedenza elettrochimica spettroscopia (EIS) (da 1000 kHz a 0,1 Hz con ampiezza potenziale di 5 mV) e le misurazioni della voltammetria ciclica (CV) dei campioni sono state effettuate su Stazione elettrochimica biologica VMP3. Carica/scarica galvanostatica (GCD) la misurazione del MoO3/LiSiON/Li TFLB è stata effettuata utilizzando un Neware BTS4000 sistema di batterie in un vano portaoggetti riempito di argon a temperatura ambiente. Un Sartorio Per determinare è stata utilizzata la bilancia analitica (CPA225D, con risoluzione di 10 μg) il carico di massa dell'elettrodo e il carico di massa della pellicola di MoO3 lo sono circa 0,4 mgâcm-2.
2 Risultati e discussione
Come mostrato nell'immagine ottica inserita nella Fig. 1(a), a Il target Li2SiO3 è stato utilizzato per preparare il film sottile LiSiON. Il risultato dell'XRD nella Fig. 1(a) rivela che l'obiettivo è composto dal principale Li2SiO3 (JCPDS 83-1517) e fase minore SiO2. La misurazione ICP-MS indica che l'atomo il rapporto Li:Si è di circa 1,79:1 nel target. Trasparente amorfo sottile è stata ottenuta una pellicola per il tipico campione LiSiON-100N9A1 dopo lo sputtering bersaglio (Fig. 1 (b)). Lo spessore del tipico campione LiSiON-100N9A1 misurato dal L'immagine FESEM in sezione trasversale nella Fig. 1(c) è circa 1,2 μm, indicando un tasso di crescita di circa 100 nmâh-1 sotto questa condizione. Come mostrato nell'immagine FESEM vista dall'alto nella Fig. 1(d), il la superficie del film sottile LiSiON è molto liscia e densa senza crepe o fori di spillo, che lo rendono un elettrolita solido adatto per TFLB per evitare scorciatoie e problema di sicurezza.
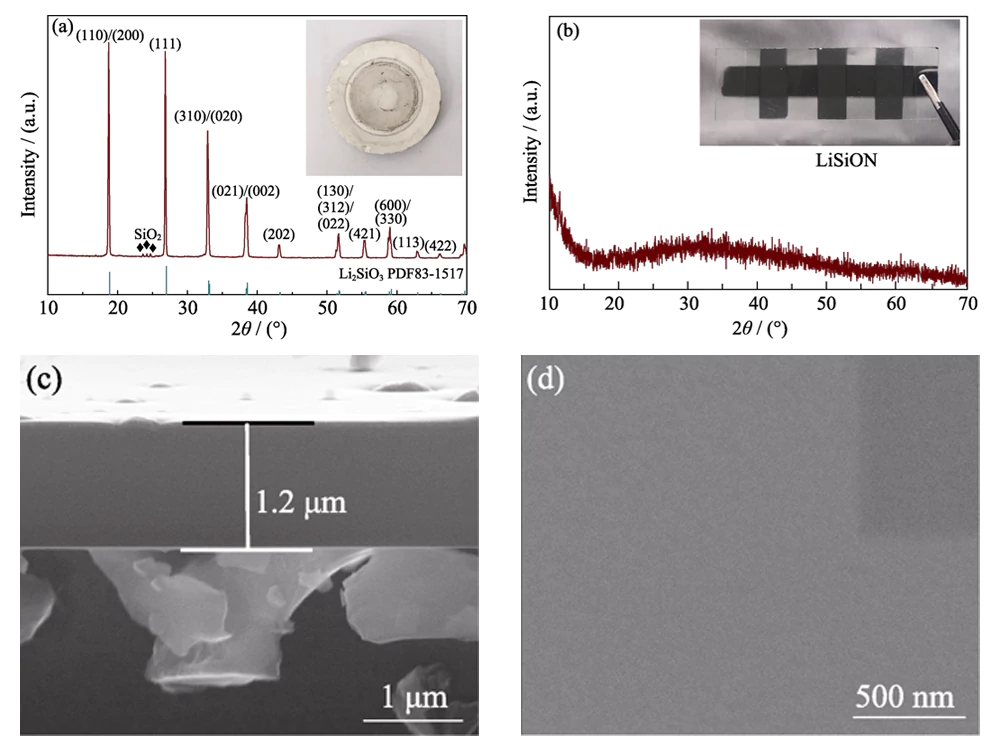
Fig. 1 (a) Modello XRD e immagine ottica del bersaglio Li2SiO3; (b) Modello XRD e immagine ottica di campione tipico LiSiON-100N9A1; (c) Immagini FESEM in sezione trasversale e (d) vista dall'alto del tipico campione LiSiON-100N9A1
L'analisi XPS è stata effettuata per studiare la composizione chimica e informazioni sul legame del target Li2SiO3 e del tipico campione LiSiON-100N9A1. L'indagine XPS spettri di scansione nella Fig. 2(a) rivelare la presenza di elementi Li, Si e O nel bersaglio Li2SiO3 e l'introduzione dell'elemento N nel film sottile LiSiON. Il rapporto atomico di N: Il Si nel film sottile LiSiON è di circa 0,33: 1 secondo il risultato XPS. Combinando con il corrispondente rapporto atomico (1,51:1) ottenuto dall'ICP-MS misurazione, la stechiometria del tipico campione LiSiON-100N9A1 è determinato essere Li1.51SiO2.26N0.33. Rispetto al singolo picco Si-Si (103,2 eV) nel Spettro XPS Si2p a livello core del target Li2SiO3 (Fig. 2(b)), è possibile osservare un picco aggiuntivo di Si-N (101,6 eV) dal film sottile LiSiON, suggerendo la presenza di nitrurazione nel LiSiON[11,12]. Gli O1 spettro XPS a livello centrale del target Li2SiO3 nella Fig. 2 (c) mostra due ambienti di legame: 531,5 eV originato da SiOx e 528,8 eV assegnato a Li2O. Dopo la deposizione, è emersa una componente aggiuntiva a 530,2 eV può essere osservato con il film sottile LiSiON, che può essere assegnato al non-bridging ossigeno (On) nel silicato[13,14]. Lo spettro XPS di livello core N1 del film sottile LiSiON nella Fig. 2(d) can essere deconvoluto in tre picchi, inclusi 398,2 eV per il legame Si-N, 396,4 eV per Li3N e 403,8 eV per la specie nitrito NO2-, confermando ulteriormente l'incorporazione di N nella Rete LiSiON[14,15,16]. Come illustrato schematicamente nella Fig. 2(e), il l'incorporazione di N nella rete LiSiON può formare più legami incrociati struttura, che è vantaggiosa per la rapida conduzione degli ioni di litio[6,17].
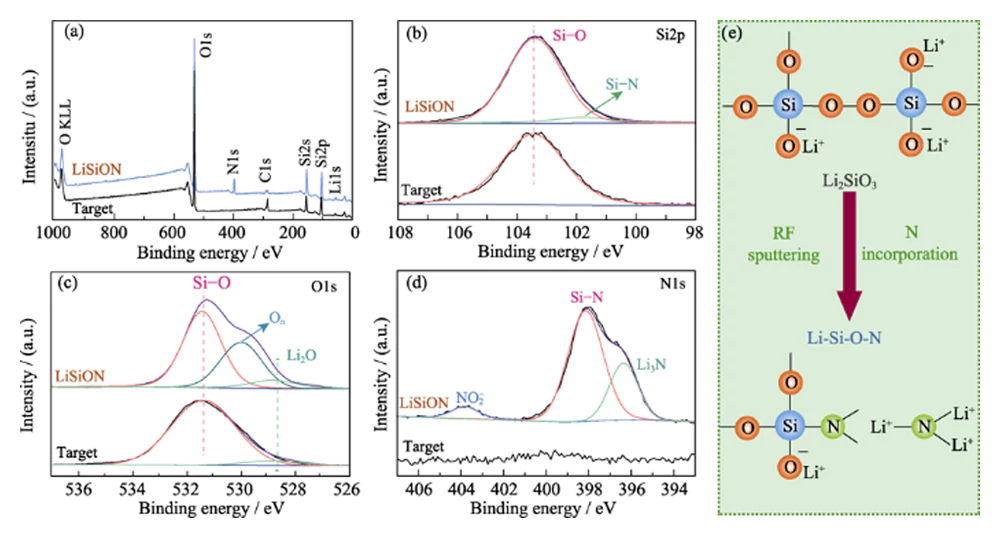
Fig. 2 (a) Survey-scan, (b) Si2p a livello core, (c) O1s a livello core, e (d) spettri XPS a livello centrale N1 del target Li2SiO3 e del campione tipico LiSiON-100N9A1; (e) Illustrazione schematica del cambiamento parziale della struttura da Li2SiO3 a LiSiON con l'incorporazione di N
Per ottimizzare la conduttività ionica e la stabilità elettrochimica del Film sottili di LiSiON, vari film sottili di LiSiON depositati con diversi sputtering potenze e flussi di gas di lavoro sono stati confrontati in termini di ioni conduttività e finestre di tensione. Le trame Nyquist a temperatura ambiente del I film sottili LiSiON sono mostrati nella Fig. 3(a) e la corrispondente struttura sandwich Pt/LiSiON/Pt e il circuito equivalente lo sono mostrato nella Fig. 3(b). COME osservato, i grafici di Nyquist mostrano un singolo semicerchio e dielettrico coda di capacità, che è caratteristica del dielettrico conduttore a film sottile con processo di rilassamento in massa inserito tra i contatti di blocco[17]. Lo ionico le conduttività (Ïi) dei film sottili LiSiON possono essere calcolate utilizzando l'Eq. (1).
Ïi=d/(RA)
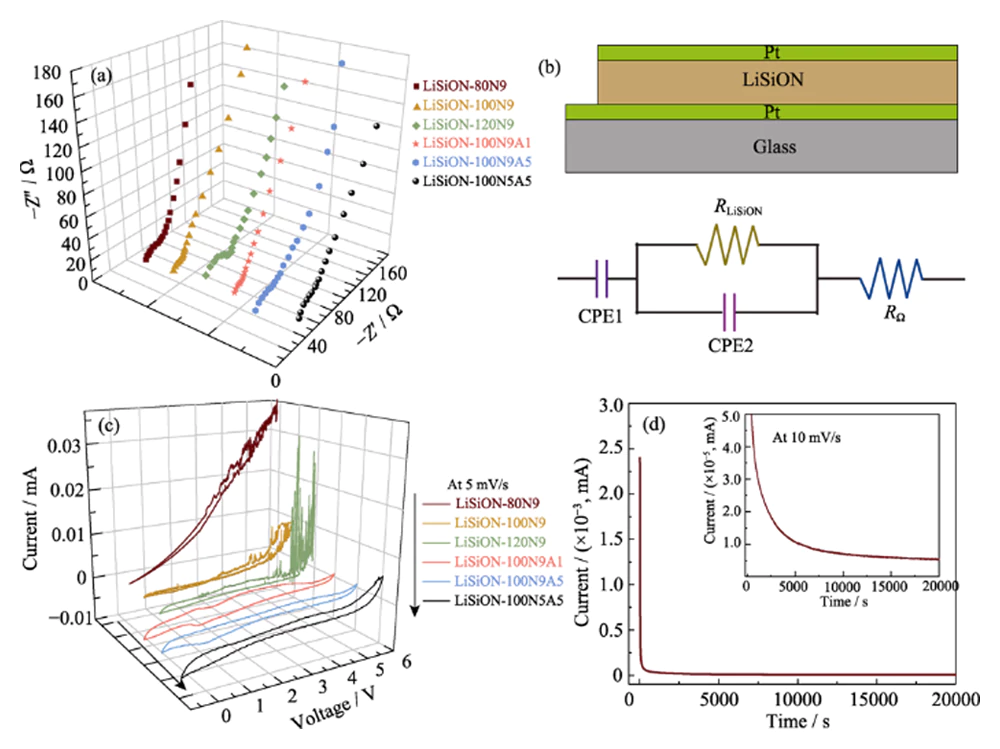
Fig. 3 (a) Spettri di spettroscopia di impedenza elettrochimica (EIS) di i film sottili LiSiON depositati in diverse condizioni; (b) Schema illustrazione della struttura sandwich Pt/LiSiON/Pt e la corrispondente circuito equivalente; (c) Curve CV dei film sottili LiSiON depositati sotto condizioni diverse; (d) Curva cronoamperometrica del campione LiSiON-100N9A1
dove d è lo spessore del film, A è il area effettiva (circa 1 cm2) e R è la resistenza stimata della pellicola dal diagramma di Nyquist misurato. Le conduttività ioniche calcolate per questi I film sottili LiSiON vengono confrontati nella Tabella 1. Come osservato, la conduttività ionica del film sottile LiSiON depositato a un flusso costante di 90 sccm N2 aumenta con l'aumento della potenza di sputtering da 80 W a 100 W, per poi diminuire quando la potenza di sputtering viene ulteriormente elevata a 120 W, che è simile al precedente rapporto sull'elettrolita LiPON[18]. Un ovvio l'incremento della conduttività ionica può essere osservato quando il rapporto N2 è in viene promosso il gas di lavoro con una potenza di sputtering costante di 100 W, il che può essere attribuito alla maggiore quantità di azoto incorporato nel LiSiON con un ambiente più favorevole per il movimento degli ioni di litio[5, 18]. Notevolmente, il campione LiSiON-100N9 e LiSiON-100N9A1 mostrano il valore ionico più elevato conduttività rispettivamente di 7,1×10-6 e 6,3×10-6 Sâcm-1, che sono ovviamente più elevate rispetto al noto LiPON (~2Ã10-6 Sâcm-1), il LiNbO3 amorfo precedentemente riportato (~1Ã10-6 Sâcm-1)[19], il LiBON (2.3Ã10- 6 Sâcm-1)[20], Li-V-Si-O (~1×10-6 Sâcm-1)[21], Li-La-Zr-O (4×10-7 Sâcm-1)[22] e Li-Si-P-O (1,6×10-6 Sâcm-1)[23] film elettrolitici, rivelando che l'amorfo Il film sottile LiSiON è un candidato competitivo come elettrolita per TFLB. L'alto la conduttività ionica del film sottile LiSiON può essere attribuita all'incorporazione di N nel film sottile e la formazione di legami Si-N invece di legami Si-O, portando a una rete anionica più reticolata per il facile ione litio mobilità[17, 24]. Le finestre di tensione elettrochimicamente stabili del LiSiON i film sottili sono stati valutati mediante misurazione CV a una velocità di scansione di 5 mVâs-1 con tensione fino a 5,5 V. Va sottolineato che l'impatto della deposizione le condizioni sulla finestra di tensione delle pellicole LiSiON variano, il che non può essere spiegato da un meccanismo chiaro attualmente poiché non ci sono ricerche pertinenti in precedenti rapporti sull'elettrolita a film sottile[18,24-25]. Tuttavia, rispetto alla Fig. 3(c) e nella Tabella 1, i campioni LiSiON-100N9A1 e LiSiON-100N5A5 mostrano la tensione più ampia windows di ~5.0 e ~5.2 V, rispettivamente, che sono vicini a quelli del LiPON elettrolita. Pertanto, sono state prese sia la conduttività ionica che la finestra di tensione in considerazione, il campione LiSiON-100N9A1 è stato scelto per ulteriori indagini e la fabbricazione di celle complete. Esplorare il trasferimento degli ioni di litio numero (Ïi) e la conduttività elettronica (Ïe) del campione LiSiON-100N9A1, la cronoamperometria è stata ulteriormente eseguita a tensione costante di 10 mV (Fig. 3 (d)). La Ïi può essere calcolata dall'Eq. (2).
Ïi=(Ib-Ie)/Ib
dove Ib è la corrente di polarizzazione iniziale e Ie è quella stabile stato attuale[18]. L'Ïi è stato calcolato pari a 0,998, ovvero vicino a 1, indicando che la conduzione degli ioni litio è assolutamente dominante nell'elettrolito. L'Ïi è determinato da un effetto misto di conduzione di ioni ed elettroni[24], che può essere espressa dall'Eq. (3).
Ïi=Ïi/(Ïi+Ïe)
Pertanto, l'Ïe del campione LiSiON-100N9A1 viene calcolato come 1,26×10-8 Sâcm-1, che è trascurabile rispetto alla sua conduttività ionica.
Tabella 1 Confronto tra conduttività e tensione degli ioni di litio finestre di film sottili LiSiON depositati in diverse condizioni
|
Esempio |
Conduttività degli ioni di litio |
Tensione |
|
LiSiON-80N9 |
4.6 |
~2.0 |
|
LiSiON-100N9 |
7.1 |
~3.9 |
|
LiSiON-120N9 |
2,5 |
~4.2 |
|
LiSiON-100N9A1 |
6.3 |
~5.0 |
|
LiSiON-100N9A5 |
3.0 |
~4.6 |
|
LiSiON-100N5A5 |
2.9 |
~5.2 |
Verificare la fattibilità del campione ottimizzato LiSiON-100N9A1 per Applicazione TFLB, MoO3/LiSiON/Li TFLB è stata ulteriormente fabbricata. La sezione trasversale Immagine FESEM e corrispondenti immagini di mappatura EDS del MoO3/LiSiON/Li TFLB sono mostrati nella Fig. 4(a). COME osservato, il catodo di MoO3 (circa 1,1 μm di spessore) e l'anodo di Li sono ben separati dall'elettrolita LiSiON e l'elettrolita LiSiON ha interfacce a stretto contatto sia con il catodo che con l'anodo. Figura 4(b) visualizza la curva CV tipica del TFLB a una velocità di scansione di 0,1 mVâs-1 tra 1,5-3,5 V, che mostra una coppia di picchi redox ben definiti intorno a 2,25 e 2,65 V, corrispondente all'inserimento e all'estrazione degli ioni di litio dal MoO3[10]. Figura 4(c) raffigura le prime 3 curve di carica/scarica galvanostatiche del TFLB in a densità di corrente di 50 mAâg-1 (20 μAâcm-2, in base alla massa della pellicola di MoO3). Come osservato, il TFLB mantiene i risultati la capacità di carica/scarica iniziale è di 145/297 mAhâg-1 (58/118,8 μAhâcm-2). Dopo il 2° ciclo, comportamento ciclico stabile con elevata reversibilità la capacità specifica di 282 mAhâg-1 è stata raggiunta dal TFLB. L'andamento del tasso di il TFLB a varie densità di corrente è illustrato nella Fig. 4(d). IL perdita irreversibile di capacità del TFLB nei primi cicli a bassa corrente la densità può essere attribuita alla transizione di fase irreversibile nel MoO3 derivato mediante inserimento di litio[26]. Capacità di scarico stabili di circa 219, 173, 107 e 50 mAhâg-1 si osservano rispettivamente a 100, 200, 400 e 800 mAâg-1, dimostrando una buona capacità tariffaria. Valutare la stabilità elettrochimica del TFLB, le prestazioni del ciclo sono state ulteriormente eseguite con una densità di corrente di 200 mAâg-1 (Fig. 4(e)). Il TFLB può conservare il 78,1% della sua capacità di scarica iniziale dopo 200 cicli, e l'efficienza Coulombiana è prossima al 100% per ogni ciclo, rivelandosi accettabile stabilità elettrochimica dell'elettrolita LiSiON. Le misurazioni EIS erano ulteriormente effettuato a tensione a circuito aperto per indagare il interfaccia elettrolita/elettrodo nel TFLB a diversi numeri di ciclo e il i corrispondenti grafici di Nyquist con circuito equivalente sono rappresentati nella Fig. 4(f). COME osservato, il TFLB MoO3/LiSiON/Li mostra uno spettro EIS simile che consiste di due semicerchi nella regione delle alte frequenze allo stato fresco a quella del MoO3/LiPON/Li TFLB nel nostro lavoro precedente[10], indicando che la resistenza interfacciale Li/LiSiON è trascurabile rispetto a quella del Interfaccia LiSiON/MoO3[20]. Il primo piccolo semicerchio nelle trame di Nyquist è attribuito alla conduzione ionica degli ioni Li+ nell'elettrolita LiSiON, mentre il il secondo grande semicerchio corrisponde al processo di trasferimento di carica nel Interfaccia LiSiON/MoO3[27,28]. Si noti che il primo piccolo semicerchio raramente cambiamenti durante i cicli, indicando la stabilità ciclica relativamente buona di l'elettrolita LiSiON. Tuttavia, il secondo semicerchio si espande gradualmente man mano che il il numero di cicli si evolve, rivelando la maggiore interfaccia LiSiON/MoO3 resistenza durante il ciclismo, che potrebbe essere la ragione principale della capacità sbiadimento del TFLB[29]. Vale la pena ricordare che questo funziona con successo adotta l'elettrolita LiSiON per costruire TFLB e dimostra il buono contatto interfacciale di LiSiON sia con il catodo MoO3 che con l'anodo di litio per prima volta. Inoltre, la grande capacità specifica, la buona capacità tariffaria e le prestazioni del ciclo accettabili del MoO3/LiSiON/Li TFLB dimostrano che il LiSiON il film sottile è ben applicabile come elettrolita per TFLB.
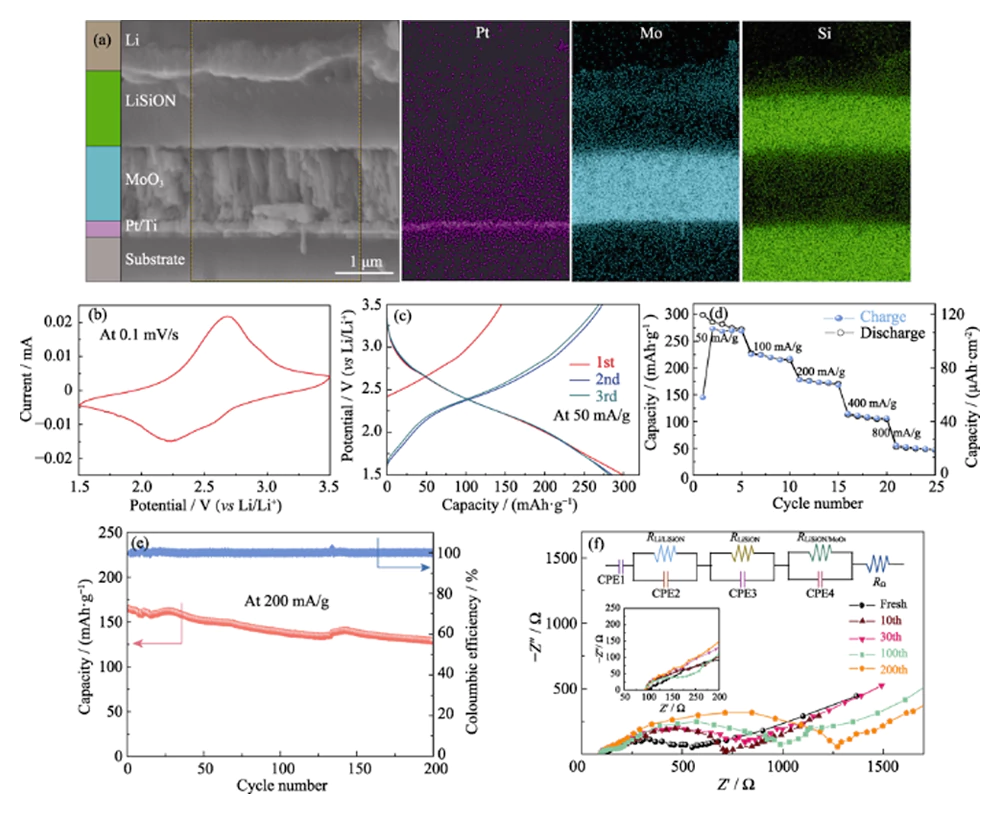
Fig. 4 (a) Immagine FESEM in sezione trasversale e corrispondente mappatura EDS immagini del MoO3/LiSiON/Li TFLB; (b) Curva CV tipica, (c) tre curve iniziali di carica/scarica, (d) velocità prestazioni, (e) prestazioni del ciclo e (f) spettri EIS a cicli diversi numeri del MoO3/LiSiON/Li TFLB con campione LiSiON-100N9A1 come elettrolita
3 Conclusioni
In sintesi, l'elettrolita amorfo a film sottile LiSiON ha avuto successo preparato mediante sputtering di magnetron RF utilizzando un target Li2SiO3 con flusso di gas N2/Ar. Il film sottile LiSiON ottimizzato depositato sotto una potenza RF di 100 W al flusso di 90 sccm N2 e 10 sccm Ar possiedono superficie liscia, struttura densa, alto contenuto di ioni conduttività (6,3×10-6 Sâcm-1) e un'ampia finestra di tensione (5 V), che lo rendono un promettente materiale elettrolitico per TFLB. Ancora più importante, utilizzando LiSiON elettrolita, un TFLB MoO3/LiSiON/Li è stato dimostrato con successo per il prima volta con elevata capacità specifica (282 mAhâg-1 a 50 mAâg-1), buone prestazioni in termini di velocità (50 mAhâg-1 a 800 mAâg-1) e stabilità del ciclo accettabile (ritenzione della capacità del 78,1% dopo 200 cicli). Ci si aspetta che questo lavoro offra nuove opportunità per sviluppare TFLB ad alte prestazioni utilizzando un elettrolita a film sottile basato su Li2O-SiO2.
Riferimenti
[1] MOITZHEIM S, PUT B, VEREECKEN P M. Progressi nelle batterie agli ioni di litio a film sottile 3D. Interfacce dei materiali avanzati, 2019,6(15):1900805.
[2] XIA Q, ZHANG Q, SUN S, et al. Array di nanofogli LixMnO2 a tunnel intercrescitato come catodo 3D per microbatterie al litio a film sottile interamente a stato solido ad alte prestazioni. Materiali avanzati, 2021,33(5):2003524.
[3] DENG Y, EAMES C, FLEUTOT B, et al. Miglioramento della conduttività degli ioni di litio negli elettroliti solidi con conduttore superionico di litio (LISICON) attraverso un effetto misto di polianioni. Materiali e interfacce applicati ACS, 2017,9(8):7050-7058.
[4] BATES J B, DUDNEY N J, GRUZALSKI G R, et al. Fabbricazione e caratterizzazione di film sottili di elettrolita di litio amorfo e batterie ricaricabili a film sottile. Journal of Power Sources, 1993,43(1/2/3):103-110.
[5] BATES J. Proprietà elettriche dei film sottili di elettrolita di litio amorfo. Solid State Ionics, 1992,53(56):647-654.
[6] FAMPRIKIS T, GALIPAUD J, CLEMENS O, et al. Dipendenza dalla composizione della conduttività ionica negli elettroliti a film sottile LiSiPO(N) per batterie allo stato solido. ACS Materiali energetici applicati, 2019,2(7):4782-4791.
[7] DENG Y, EAMES C, CHOTARD J N, et al. Approfondimenti strutturali e meccanicistici sulla conduzione rapida degli ioni di litio negli elettroliti solidi Li4SiO4-Li3PO4. Giornale dell'American Chemical Society, 2015,137(28):9136-9145.
[8] CHEN R, SONG X. La conduttività ionica degli elettroliti solidi per sistemi Li4+xMxSi1-xO4-yLi2O (M=Al, B). Giornale della Società Chimica Cinese, 2002,49:7-10.
[9] ADNAN S, MOHAMED N S. Effetti della sostituzione di Sn sulle proprietà dell'elettrolita ceramico Li4SiO4. Solid State Ionics, 2014,262:559-562.
[10] SUN S, XIA Q, LIU J, et al. Array di nanoflake α-MoO3-x autoportanti carenti di ossigeno come catodo 3D per batterie al litio avanzate a film sottile completamente allo stato solido. Giornale di Materiomics, 2019,5(2):229-236.
[11] DING W, LU W, DENG X, et al. Uno studio XPS sulla struttura del film SiNx depositato mediante sputtering di magnetron ECR a microonde. Acta Physica Sinica, 2009,58(6):4109-4116.
[12] KIM H, KIM Y. Nitridazione parziale di Li4SiO4 e conduttività ionica di Li4. 1SiO3. 9N0. 1Ceramics International, 2018,44(8):9058-9062.
[13] MARIKO M, HIDEMASA K, TOMOYUKI O, et al. Analisi degli anodi SiO per batterie agli ioni di litio. Giornale della Società Elettrochimica, 2005,152(10):A2089.
[14] FINGERLE M, BUCHHEIT R, SICOLO S, et al. Reazione e formazione dello strato di carica spaziale sull'interfaccia LiCoO2-LiPON: approfondimenti sulla formazione dei difetti e sull'allineamento del livello di energia ionica mediante un approccio combinato di scienza e simulazione delle superfici. Materiali di chimica, 2017,29(18):7675-7685.
[15] WEST W, HOOD Z, ADHIKARI S, et al. Riduzione della resistenza al trasferimento di carica sull'interfaccia elettrolita-elettrodo solido mediante deposizione laser pulsata di pellicole da una sorgente cristallina di Li2PO2N. Journal of Power Sources, 2016,312:116-122.
[16] SICOLO S, FINGERLE M, HAUSBRAND R, et al. Instabilità interfacciale del LiPON amorfo contro il litio: una teoria del funzionale della densità combinata e uno studio spettroscopico. Journal of Power Sources, 2017,354:124-133.
[17] WU F, LIU Y, CHEN R, et al. Preparazione e prestazioni del nuovo elettrolita a film sottile Li-Ti-Si-P-O-N per batterie al litio a film sottile. Giornale delle fonti di energia, 2009,189(1):467-470.
[18] PUT B, VEREECKEN M, MEERSSCHAUT J, et al. Caratterizzazione elettrica di strati LiPON ultrasottili sottoposti a polverizzazione RF per batterie su scala nanometrica. Materiali e interfacce applicati ACS, 2016,8(11):7060-7069.
[19] NIINOMI H, MOTOYAMA M, IRIYAMA Y. Conduzione di Li+ in film di Li-Nb-O depositati con un metodo Sol-Gel. Solid State Ionics, 2016,285:13-18.
[20] SONG S, LEE K, PARK H. Microbatterie flessibili allo stato solido ad alte prestazioni basate sull'elettrolita solido di ossinitruro di boro litio. Giornale delle fonti di energia, 2016,328:311-317.
[21] OHTSUKA H, OKADA S, YAMAKI J. Batteria allo stato solido con film sottile di elettrolita solido Li2O-V2O5-SiO2. Solid State Ionics, 1990,40-41:964-966.
[22] Kalita D, Lee S, Lee K, et al. Proprietà di conducibilità ionica dell'elettrolita solido amorfo Li-La-Zr-O per batterie a film sottile. Solid State Ionics, 2012,229:14-19.
[23] SAKURAI Y, SAKUDA A, HAYASHI A, et al. Preparazione di film sottili amorfi Li4SiO4-Li3PO4 mediante deposizione laser pulsata per batterie secondarie al litio allo stato solido. Solid State Ionics, 2011,182:59-63.
[24] TAN G, WU F, LI L, et al. Preparazione mediante sputtering magnetron di elettroliti a film sottile a base di fosfato di litio-alluminio-titanio incorporati in azoto per batterie agli ioni di litio completamente allo stato solido. Il giornale di chimica fisica C, 2012,116(5):3817-3826.
[25] YU X, BATES J B, JELLISON G, et al. Un elettrolita di litio stabile a film sottile: ossinitruro di litio e fosforo. Giornale della Società Elettrochimica, 1997,144(2):524.
[26] KIM H, COOK J, LIN H, et al. I posti vacanti di ossigeno migliorano le proprietà di stoccaggio della carica pseudocapacitiva di MoO3-x. Materiali naturali, 2017,16:454-460.
[27] CANZONE H, WANG S, CANZONE X, et al. Batterie litio-aria allo stato solido alimentate dall'energia solare che funzionano a temperature estremamente basse. Scienze energetiche e ambientali, 2020,13(4):1205-1211.
[28] WANG Z, LEE J, XIN H, et al. Effetti dello strato interfacciale elettrolitico catodico (CEI) sul ciclo a lungo termine delle batterie a film sottile completamente allo stato solido. Giornale delle fonti di energia, 2016,324:342-348.
[29] QIAO Y, DENG H, HE P, et al. Una cella al litio-metallo da 500 Wh/kg basata su redox anionico. Joule, 2020,4(6):1311-1323.



