Categorie
nuovo blog
- Confronto tra i materiali catodici delle batterie: NMC vs LFP vs NCA
- Tendenze nella produzione di batterie agli ioni di litio nel 2026: una guida per gli acquirenti B2B.
- Guida dettagliata al processo di produzione delle batterie agli ioni di litio
- Principali cause di perdite nella sigillatura delle celle della tasca
- Formazione e classificazione nella produzione di batterie agli ioni di litio
Tag
Test delle prestazioni elettrochimiche di nanocubi Fe4[Fe(CN)6]3 di alta qualità
Preparazione di nanocubi Fe4[Fe(CN)6]3 di alta qualità: come materiale catodico per batterie acquose agli ioni di sodio
WANG Wu Lian. Nanocubi Fe4[Fe(CN)6]3 di alta qualità: sintesi e prestazioni elettrochimiche come materiale catodico per batterie acquose agli ioni di sodio. Journal of Inorganic Materials[J], 2019, 34(12): 1301-1308 doi:10.15541/jim20190076
Test delle prestazioni elettrochimiche di nanocubi Fe4[Fe(CN)6]3 di alta qualità
Innanzitutto, le prestazioni elettrochimiche di HQ-FeHCF e LQ-FeHCF nell'elettrolita Na-H2O-PEG sono state testate utilizzando un sistema a tre elettrodi. La Figura 4 (a) mostra le curve di voltammetria ciclica di HQ-FeHCF e LQ-FeHCF nell'elettrolita Na-H2O-PEG con una velocità di scansione di 1 mV s-1. Si può chiaramente osservare dalla figura che in HQ-FeHCF sono apparse due coppie di picchi redox indipendenti, indicando che si sono verificate due reazioni redox, corrispondenti all'intercalazione/deintercalazione reversibile di due Na+. La prima coppia di picchi redox è apparsa a 0,03 e 0,28 V, corrispondenti alla riduzione e all'ossidazione degli ioni FeIII/FeII ad alto spin attaccati agli atomi di carbonio. La seconda coppia di picchi redox appare a 1,12 e 1,26 V, corrispondente alla riduzione e all'ossidazione degli ioni FeIII/FeII a basso spin legati agli atomi di azoto. Alla stessa velocità di scansione,
La Figura 4 (b) mostra le curve di carica-scarica a corrente costante di HQ-FeHCF e LQ-FeHCF a 1C (1C= 120 mA g-1) rate. Si può vedere chiaramente dalla figura che HQ-FeHCF ha due plateau di tensione durante il processo di carica e scarica, indicando che l'inserimento/estrazione di Na+ è completato in due fasi. Ciò corrisponde alle due coppie di picchi redox che appaiono in Fig. 4 (a). LQ-FeHCF mostra curve di carica-scarica simili a HQ-FeHCF, ma la sua capacità di scarica è significativamente inferiore a quella di HQ-FeHCF.
La Figura 4 (c) mostra le prestazioni del tasso di HQ-FeHCF e LQ-FeHCF. Si può vedere dalla figura che le capacità specifiche di HQ-FeHCF a velocità 1C, 2C, 5C, 10C, 20C, 30C e 40C sono 124, 118, 105, 94, 83, 74 e 63 mAh·g-1, rispettivamente. Vale la pena notare che tornando nuovamente a 1C, la capacità è tornata a 124 mAh·g-1, mostrando prestazioni di velocità eccellenti. Ci sono due ragioni per cui HQ-FeHCF ha prestazioni così buone: in primo luogo, il materiale HQ-FeHCF sintetizzato con il metodo in questo documento ha un'alta qualità e pochi difetti di posto vacante, garantendo così il trasporto efficiente di Na+. In secondo luogo, l'ampia struttura a canali del materiale accorcia il percorso di trasporto del Na+. Inoltre, la struttura di HQ-FeHCF sintetizzata lentamente aggiungendo PVP è molto stabile e i cicli di carica-scarica ad alta velocità non porteranno al collasso strutturale di HQ-FeHCF, con conseguente degrado delle prestazioni elettrochimiche. Le capacità specifiche di LQ-FeHCF a velocità 1C, 2C, 5C, 10C, 20C, 30C e 40C sono rispettivamente 112, 104, 81, 59, 35, 18 e 7 mAh·g-1. La performance complessiva del tasso è peggiore di quella di HQ-FeHCF, specialmente a tassi elevati, il divario è particolarmente evidente. Questo perché LQ-FeHCF non ha una struttura stabile e ci sono un gran numero di difetti di vacanza [Fe (CN) 6] e acqua cristallina nel suo cristallo, che ostacolano la deintercalazione di Na +, con conseguente capacità specifica estremamente bassa di LQ -FeHCF ad alti ingrandimenti. soprattutto a tassi elevati, il divario è particolarmente evidente. Questo perché LQ-FeHCF non ha una struttura stabile e ci sono un gran numero di difetti di vacanza [Fe (CN) 6] e acqua cristallina nel suo cristallo, che ostacolano la deintercalazione di Na +, con conseguente capacità specifica estremamente bassa di LQ -FeHCF ad alti ingrandimenti. soprattutto a tassi elevati, il divario è particolarmente evidente. Questo perché LQ-FeHCF non ha una struttura stabile e ci sono un gran numero di difetti di vacanza [Fe (CN) 6] e acqua cristallina nel suo cristallo, che ostacolano la deintercalazione di Na +, con conseguente capacità specifica estremamente bassa di LQ -FeHCF ad alti ingrandimenti.
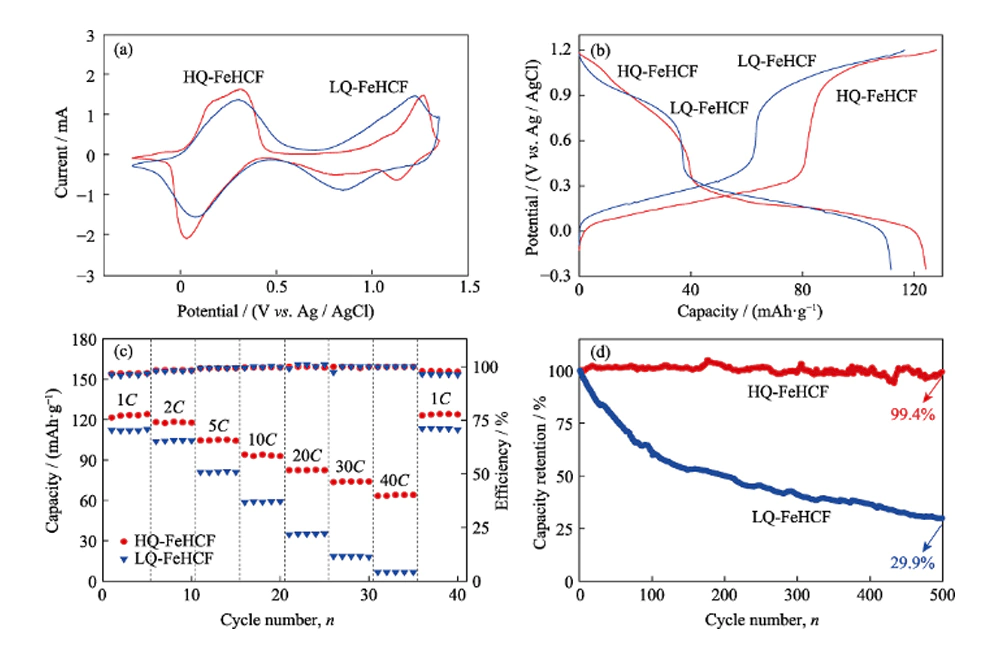
Fig. 4 (a) Curve del voltammogramma ciclico (CV) di HQ-FeHCF e LQ-FeHCF alla velocità di sweep di 1 mV·s-1 nell'elettrolita di Na-H2O-PEG; (b) Curve di carica e scarica di HQ-FeHCF e LQ-FeHCF a 1C; (c) Andamento del tasso di HQ-FeHCF e LQ-FeHCF; (d) Prestazioni cicliche di HQ-FeHCF e LQ-FeHCF
La stabilità ciclica è un parametro importante per le batterie acquose agli ioni di Na nelle applicazioni pratiche. Le prestazioni cicliche di HQ-FeHCF e LQ-FeHCF a velocità 5C sono mostrate in Fig. 4 (d). La capacità di scarica di LQ-FeHCF nel primo ciclo è di 87 mAh·g-1, ma la sua capacità diminuisce rapidamente con l'aumentare dei tempi di ciclo. Dopo 100 cicli, il tasso di mantenimento della capacità era del 61% e dopo 500 cicli, la capacità era di soli 26 mAh·g-1, corrispondente a un tasso di mantenimento della capacità del 29,9%. HQ-FeHCF mostra una stabilità del ciclo estremamente eccellente. Dopo 100 cicli, la capacità di HQ-FeHCF non è diminuita in modo significativo, mantenendo un tasso di ritenzione della capacità del 100% e il tasso di ritenzione della capacità era ancora del 99,4% fino al 500° ciclo.
Per verificare ulteriormente la stabilità di HQ-FeHCF nell'elettrolita Na-H2O-PEG, gli elettrodi dopo 100 cicli e 500 cicli sono stati osservati mediante SEM. Come mostrato nella Figura 5, la Figura 5 (a~b) è la foto SEM di HQ-FeHCF nell'elettrolita Na-H2O-PEG dopo 100 volte di carica e scarica a corrente costante a 5°C. Si può vedere chiaramente dalla figura che ogni particella nanocubo HQ-FeHCF mantiene un alto grado di integrità, quasi nessun danno strutturale e nessun difetto sulla superficie della particella. La Figura 5 (c ~ d) sono foto SEM di HQ-FeHCF nell'elettrolita Na-H2O-PEG dopo 500 cariche e scariche a corrente costante a 5°C. Ogni particella nanocube HQ-FeHCF mantiene anche un alto grado di integrità senza alcuna deformazione strutturale o collasso. L'espansione polare dopo 500 cicli è stata sottoposta al test TG, come mostrato in Figura 6. Il contenuto di acqua di cristallizzazione di HQ-FeHCF era del 13%, nessun cambiamento significativo rispetto a prima del ciclo; il contenuto di acqua cristallina di LQ-FeHCF era del 20%, con un aumento del 2% rispetto a prima del ciclo.

Fig. 5 Immagini SEM di HQ-FeHCF dopo (ab)100 e (cd) 500 cicli
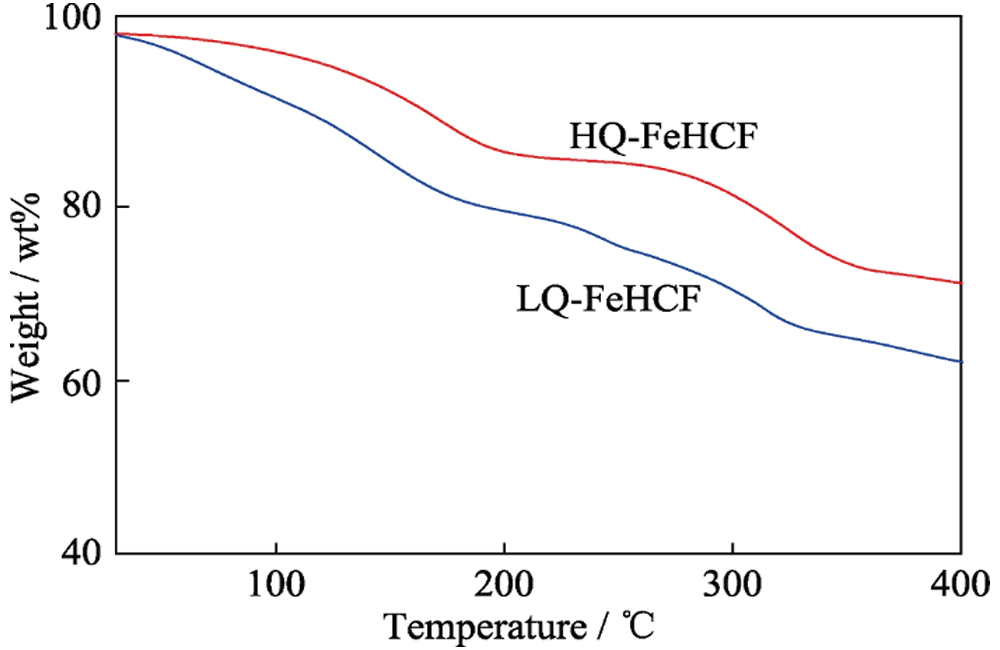
Fig. 6 Curve TG di HQ-FeHCF e LQ-FeHCF dopo 500 cicli
Il meccanismo di transizione di fase del materiale HQ-FeHCF durante la reazione elettrochimica è stato studiato mediante tecnica XRD ex-situ. La Figura 7 mostra i modelli XRD del materiale in diversi stati di carica e scarica, a~e sono il processo di carica, f~i sono il processo di scarica e i punti sono contrassegnati con picchi di diffrazione Ti. Prendendo come esempio il gruppo di picchi di diffrazione nella casella tratteggiata, si può vedere chiaramente dalla figura che i picchi di diffrazione XRD si spostano nella direzione dell'aumento di 2θ durante il processo di a~e, da 24,3° a 24,6°. Ciò è dovuto alla contrazione del reticolo causata dall'estrazione di Na+ da HQ-FeHCF durante il processo di carica. La variazione di volume della cella unitaria durante questo processo è di circa l'8,1%. Durante il processo f~i, il picco di diffrazione XRD si sposta nella direzione della diminuzione di 2θ e ritorna a 24. 3° ancora. Questo perché Na+ si reintercala in HQ-FeHCF durante il processo di scarica, provocando l'espansione del reticolo. Vale la pena notare che le posizioni dei picchi di diffrazione a e i sono altamente coincidenti. Ciò indica che la deintercatura di Na+ nel materiale HQ-FeHCF è altamente reversibile e la deintercatura reversibile di Na+ non distruggerà la struttura cristallina del materiale. Mostra anche che HQ-FeHCF ha un'elevata stabilità nell'elettrolita Na-H2O-PEG.
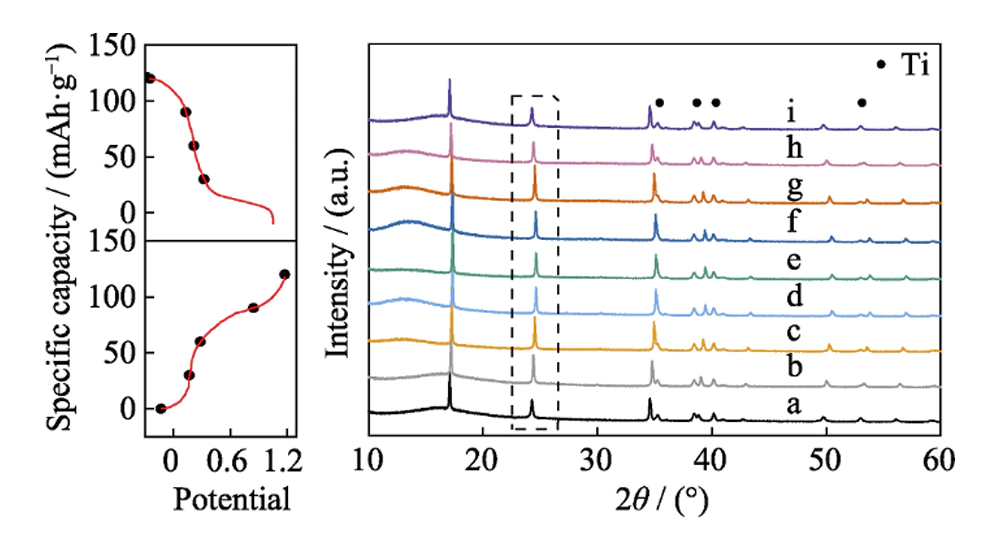
Fig. 7 Modelli XRD ex situ di materiale HQ-FeHCF in vari stati di carica e scarica
Il NaTi2(PO4)3 di tipo NASICON ha una struttura tridimensionale aperta adatta alla diffusione degli ioni sodio. Pertanto, NaTi2(PO4)3 può essere utilizzato non solo come materiale per elettrodi per batterie organiche agli ioni di sodio, ma anche come materiale per elettrodi per batterie acquose agli ioni di sodio. NaTi2(PO4)3 è stato preparato con un metodo precedente e le sue proprietà elettrochimiche nell'elettrolita Na-H2O-PEG sono state studiate mediante voltammetria ciclica (CV) e scarica di carica galvanostatica. La Figura 8(a) mostra la curva CV di NaTi2(PO4)3 a una velocità di scansione di 1 mV s-1, con una coppia di picchi redox netti a -0,64 e -0,79 V (rispetto ad Ag/AgCl). Ciò corrisponde all'intercalazione/estrazione di Na+, accompagnata dalla conversione reversibile tra Ti3+ e Ti4+. La distribuzione della tensione di NaTi2(PO4)3 è mostrata nella Figura 8(b). La piattaforma a scarica piatta a -0,69 V (vs.
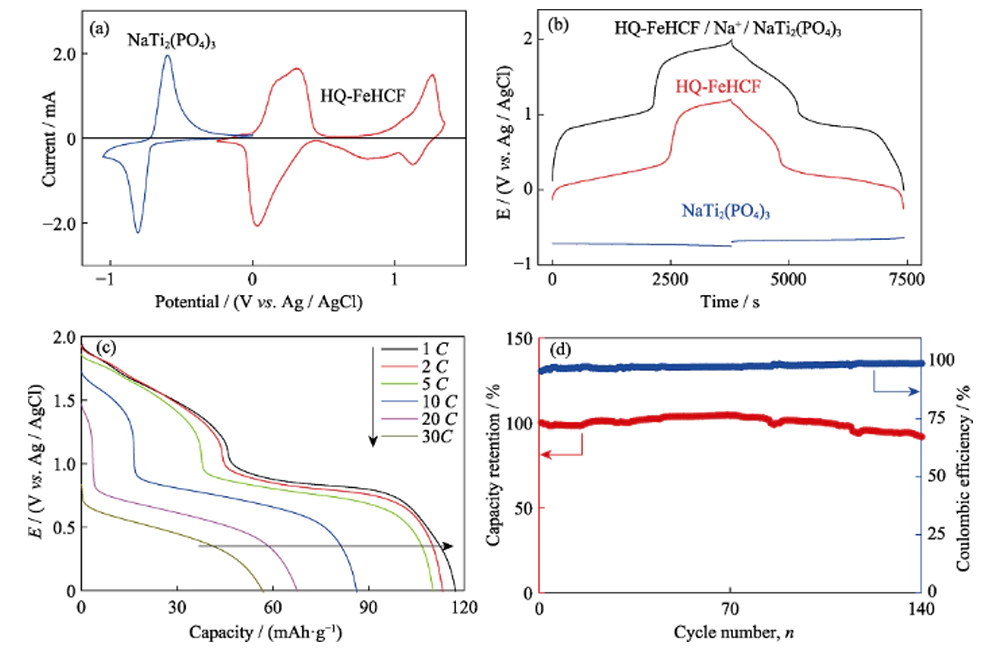
Fig. 8 (a) Curve del voltammogramma ciclico (CV) di HQ-FeHCF e NaTi2(PO4) alla velocità di sweep di 1 mV·s-1 nell'elettrolita di Na-H2O-PEG; (b) Profili di carica-scarica galvanostatica a 1C per cella intera, catodo e anodo nell'elettrolita di Na-H2O-PEG; (c) Prestazioni valutarie e (d) prestazioni ciclistiche della cella intera
Buone prestazioni elettrochimiche basate su HQ-FeHCF e NaTi2(PO4)3. Abbiamo assemblato una batteria acquosa agli ioni di sodio con HQ-FeHCF come elettrodo positivo, NaTi2(PO4)3 come elettrodo negativo e NaClO4-H2O-PEG come elettrolita. La Figura 8 (b) mostra le curve di tensione dell'elettrodo positivo, dell'elettrodo negativo e della batteria piena a una velocità di 1C. Si può vedere dalla figura che la tensione di lavoro della batteria completa è pari a 1,9 V. Un'elevata tensione di lavoro contribuisce a migliorare la densità di energia della batteria completa e la densità di energia della batteria completa calcolata in base al la massa del materiale attivo arriva fino a 126 Wh kg-1. Supera la densità di energia della maggior parte delle celle piene di ioni Na acquose precedentemente riportate utilizzando ossido di manganese, fosfato e blu di Prussia come materiali catodici. Il confronto specifico è mostrato nella Tabella 3. Come mostrato nella Fig. 8 (c), al tasso di 1C, 2C, 5C, 10C, 20C e 30C, le capacità della batteria piena sono 117, 113, 110, 86, 68 e 57 mAh·g-1, rispettivamente, che mostrano prestazioni di velocità eccellenti. La figura 8 (d) mostra le prestazioni del ciclo della batteria completa a una velocità di 5 °C. Nei primi 70 cicli, la capacità della batteria piena aumenta leggermente e l'efficienza coulombiana aumenta gradualmente dal 96% del primo ciclo a un livello vicino al 100%. Nei successivi 70 cicli, la capacità ha iniziato a diminuire lentamente, fino al 140° ciclo, il tasso di ritenzione della capacità della batteria piena è stato del 92% e l'efficienza coulombiana è rimasta vicina al 100%. Sebbene la tensione di carica di interruzione della batteria piena sia pari a 2 V, superando di gran lunga la tensione di decomposizione teorica dell'acqua (1,23 V),
Tabella 3 Densità di energia di diverse batterie acquose agli ioni di sodio
| Catodo |
Un cennoe |
Densità energetica / (Wh·kg-1) |
Rif. |
| Na0.44MnO2 |
NaTi2(PO4)3 |
33 |
[39] |
| Na2Ni[Fe(CN)6] |
NaTi2(PO4)3 |
43 |
[13] |
| Na2Cu[Fe(CN)6] |
NaTi2(PO4)3 |
48 |
[40] |
| NaMnO2 |
NaTi2(PO4)3 |
30 |
[12] |
| K0.27MnO2 |
NaTi2(PO4)3 |
55 |
[41] |
| NaFePO4 |
NaTi2(PO4)3 |
61 |
[42] |
| Na2VTi(PO4)3 |
NaTi2(PO4)3 |
68 |
[43] |
| Na3MnTi(PO4)3 |
NaTi2(PO4)3 |
82 |
[44] |
| Na0.66Mn0.66Ti0.34O2 |
NaTi2(PO4)3 |
76 |
[45] |
| Na2Ni0.4Co0.6[Fe(CN)6] |
NaTi2(PO4)3 |
121 |
[46] |
| Fe4[Fe(CN)6]3 |
NaTi2(PO4)3 |
126 |
Questo lavoro |
Conclusione
In questo studio, i nanomateriali Fe4[Fe(CN)6]3 di alta qualità ea basso difetto sono stati sintetizzati con successo mediante un metodo idrotermale semplice e conveniente. I risultati del test XRD mostrano che il materiale è una struttura cubica a facce centrate (fcc), che appartiene al gruppo di punti spaziali Fm-3m. I risultati dei test SEM e TEM mostrano che il Fe4[Fe(CN)6]3 sintetizzato ha un'eccellente cristallinità e il materiale ha una tipica struttura cubica con una lunghezza laterale di circa 500 nm. La superficie del materiale è liscia e uniforme senza gravi accumuli. Rispetto al Fe4[Fe(CN)6]3 di bassa qualità sintetizzato con metodi tradizionali. Il Fe4[Fe(CN)6]3 sintetizzato in questo documento può ridurre efficacemente i difetti di vacanza e regolare l'acqua cristallina nel materiale, in modo che il materiale abbia eccellenti prestazioni elettrochimiche: La capacità specifica a velocità 1C è pari a 124 mAh·g-1 e la capacità specifica a velocità 2C, 5C, 10C, 20C, 30C e 40C è 124, 118, 105, 94, 83, 74 e 64 mAh· g-1, rispettivamente, mostrando eccellenti prestazioni di velocità. Dopo 500 cicli a una velocità di 5°C, il tasso di ritenzione della capacità è vicino al 100%, mostrando un'eccellente stabilità del ciclo. La tensione di funzionamento della batteria completa con Fe4[Fe(CN)6]3 e fosfato di sodio e titanio come elettrodi positivi e negativi è pari a 1,9 V e la densità di energia può raggiungere i 126 Wh kg-1. Dopo 140 volte di carica e scarica a corrente costante a una velocità di 5 °C, il tasso di ritenzione della piena capacità della batteria è del 92% e l'efficienza coulombica è vicina al 100%. Il Fe4[Fe(CN)6]3 sintetizzato con questo metodo ecologico e conveniente dovrebbe essere utilizzato come materiale catodico per le batterie acquose agli ioni di Na.
Scopri di più sui materiali delle batterie agli ioni di sodio da TOB NEW ENERGY .



