Struttura di carbonio cavo drogata con cobalto come ospite di zolfo per il catodo della batteria al litio zolfo
Autore: JIN Gaoyao, HE Haichuan, WU Jie, ZHANG Mengyuan, LI Yajuan, LIU Younian. Struttura di carbonio cavo drogata con cobalto come ospite di zolfo per il catodo della batteria al litio zolfo. Journal of Inorganic Materials[J], 2021, 36(2): 203-209 DOI:10.15541/jim20200161
TOB New Energy fornisce vari materiali per batterie per batterie agli ioni di litio, batterie agli ioni di sodio , batterie al litio-zolfo, batterie allo stato solido, celle , ecc. Contattaci per un preventivo.
Sebbene le prestazioni del catodo possano essere migliorate in una certa misura con la sinergia di eteroatomi e struttura del carbonio, sono ancora significativamente limitate dalla cinetica lenta della reazione di conversione del polisolfuro, che causa l'eccessivo accumulo di LiPS e l'inevitabile diffusione. I composti dei metalli di transizione sono stati ampiamente introdotti nell'ospite di zolfo per accelerare la cinetica della reazione di conversione. Negli ultimi anni, specifiche nanoparticelle metalliche, come Co, Feand Pt, hanno mostrato un effetto accelerante simile. Tra questi metalli, il metallo cobalto ha attirato l'attenzione dei ricercatori per la sua eccellente conduttività e la forte interazione con i polisolfuri. Durante il processo di carica e scarica, può catturare efficacemente i polisolfuri e promuovere la reazione di conversione. Li, et al. ottenuto il carbonio drogato con Co e N come ospite di zolfo dalla calcinazione del precursore ZIF-67. Le nanoparticelle di Co uniformemente disperse hanno accelerato nettamente la reazione redox con l'effetto sinergico dei gruppi N-dopati. Inoltre Du, et al. ha presentato gli atomi di cobalto monodispersi incorporati nel catodo di grafene drogato con azoto e Wu, et al. fabbricato nanodots Co / carbonio mesoporoso drogato con N con la calcinazione in situ di adenina e CoCl2. In tutti questi rapporti, i sistemi Co-contained hanno ottenuto eccellenti prestazioni ciclistiche. fabbricato Co nanodots/carbonio mesoporoso drogato con N con la calcinazione in situ di adenina e CoCl2. In tutti questi rapporti, i sistemi Co-contained hanno ottenuto eccellenti prestazioni ciclistiche. fabbricato Co nanodots/carbonio mesoporoso drogato con N con la calcinazione in situ di adenina e CoCl2. In tutti questi rapporti, i sistemi Co-contained hanno ottenuto eccellenti prestazioni ciclistiche.
In questo lavoro, per migliorare le prestazioni cicliche e di velocità delle batterie Li-S, è stata progettata una struttura di carbonio cavo 3D decorata con nanoparticelle di cobalto come host del catodo di zolfo. Il citrato di sodio, un additivo economico e abbondante, viene impiegato come fonte di carbonio per il suo carattere unico durante la calcinazione diretta. E le prestazioni elettrochimiche del sistema contenente cobalto (Co/C-700) e della struttura in carbonio (HEC-700) sono state valutate sistematicamente per garantire l'effetto delle nanoparticelle di cobalto drogate per il catodo di zolfo.
1 sperimentale
1.1 Sintesi dei materiali
Tutti i reagenti chimici utilizzati in questo lavoro erano di grado analitico senza ulteriore purificazione. In breve, 0,25 g di Co(NO3)2·6H2O e 5,0 g di citrato di sodio sono stati sciolti in 20 mL di acqua deionizzata sotto agitazione magnetica per formare una soluzione omogenea. Quindi, la soluzione è stata liofilizzata, macinata in polvere fine e calcinata a 700 ℃ sotto N2 per 1 ora con una velocità di riscaldamento di 5 ℃∙min-1. I compositi ottenuti (denominati UWC-700) sono stati lavati con acqua deionizzata per 3 volte al fine di rimuovere i sottoprodotti. Dopo essere stato essiccato a 60 ℃ durante la notte, il prodotto finale è stato raccolto e indicato come Co/C-700. Per confermare ulteriormente l'effetto di Co, il carbonio inciso con acido cloridrico (HEC-700) è stato ottenuto incidendo Co/C-700 in 2 mol/L HCl per 12 ore, lavando fino a neutralità ed asciugando a 80 ℃ per 12 ore.
I compositi catodici sono stati preparati mediante un metodo convenzionale di fusione e diffusione. In breve, una miscela di zolfo (70% in peso) e compositi Co/C-700 (o HEC-700) è stata macinata per 20 minuti, trasferita in un'autoclave con contenitore in Teflon da 20 ml e riscaldata a 155 ℃ per 12 ore. La polvere ottenuta è stata raccolta come S@Co/C-700 e S@HEC-700. La caratterizzazione dei materiali e l'adsorbimento statico dei polisolfuri sono mostrati nei materiali di supporto.
1.2 Caratterizzazione elettrochimica
Le prestazioni elettrochimiche dei catodi S@Co/C-700 e S@HEC-700 sono state testate con pile a bottone tipo CR2025, fabbricate in un vano portaoggetti riempito di argon (MBraun, Germania). La sospensione catodica di zolfo è stata preparata miscelando S@Co/C-700 (o S@HEC-700), nero di acetilene e legante di polivinilidene difluoruro (PVDF) con un rapporto in peso di 7:2:1 in N-metil-2- pirrolidinone (NMP). Quindi l'impasto liquido ottenuto è stato colato uniformemente su un foglio di alluminio. Inoltre, la membrana è stata essiccata a 50 ℃ sotto vuoto durante la notte e tagliata in dischi (1 cm di diametro) con un carico di zolfo di 1,1-1,7 mg∙cm-2. La membrana di polipropilene di routine (Celgard 2400) è stata utilizzata per separare il catodo e l'anodo di litio. L'elettrolita utilizzato in ciascuna cellula era 50 μL 1mol/L di LiN(CF3SO2)2 e una soluzione di LiNO3 all'1% in peso in DOL/DME (1:1 in volume). I test di carica-scarica galvanostatici sono stati eseguiti da un sistema di test della batteria LAND CT 2001A (Jinnuo Electronic Co, Wuhan, Cina) all'interno della finestra di tensione di 1,7-2,8 V. La misurazione della voltammetria ciclica (CV) è stata eseguita da 1,5 a 3,0 V a un velocità di scansione di 0,1 mV∙s-1. La spettroscopia di impedenza elettrochimica (EIS) è stata eseguita nell'intervallo di frequenza da 0,1 MHz a 10 mHz con un'ampiezza di tensione di 5 mV a circuito aperto. Le misurazioni CV ed EIS sono state eseguite su una stazione di lavoro elettrochimica CHI 660E (Chenhua Instruments Co, Shanghai, Cina). Le celle simmetriche sono state assemblate con Co/C-700 o HEC-700 (8:2 con PVDF in rapporto in peso) come catodo e anodo identici e 50 μL di elettrolita di 1 mol/L LiN(CF3SO2)2, 1% in peso di LiNO3 e 0,2 mol/L Li2S6 in soluzione DOL/DME (1:1 in volume). Cina) entro la finestra di tensione di 1,7-2,8 V. La misurazione della voltammetria ciclica (CV) è stata eseguita da 1,5 a 3,0 V a una velocità di scansione di 0,1 mV∙s-1. La spettroscopia di impedenza elettrochimica (EIS) è stata eseguita nell'intervallo di frequenza da 0,1 MHz a 10 mHz con un'ampiezza di tensione di 5 mV a circuito aperto. Le misurazioni CV ed EIS sono state eseguite su una stazione di lavoro elettrochimica CHI 660E (Chenhua Instruments Co, Shanghai, Cina). Le celle simmetriche sono state assemblate con Co/C-700 o HEC-700 (8:2 con PVDF in rapporto in peso) come catodo e anodo identici e 50 μL di elettrolita di 1 mol/L LiN(CF3SO2)2, 1% in peso di LiNO3 e 0,2 mol/L Li2S6 in soluzione DOL/DME (1:1 in volume). Cina) entro la finestra di tensione di 1,7-2,8 V. La misurazione della voltammetria ciclica (CV) è stata eseguita da 1,5 a 3,0 V a una velocità di scansione di 0,1 mV∙s-1. La spettroscopia di impedenza elettrochimica (EIS) è stata eseguita nell'intervallo di frequenza da 0,1 MHz a 10 mHz con un'ampiezza di tensione di 5 mV a circuito aperto. Le misurazioni CV ed EIS sono state eseguite su una stazione di lavoro elettrochimica CHI 660E (Chenhua Instruments Co, Shanghai, Cina). Le celle simmetriche sono state assemblate con Co/C-700 o HEC-700 (8:2 con PVDF in rapporto in peso) come catodo e anodo identici e 50 μL di elettrolita di 1 mol/L LiN(CF3SO2)2, 1% in peso di LiNO3 e 0,2 mol/L Li2S6 in soluzione DOL/DME (1:1 in volume). La spettroscopia di impedenza elettrochimica (EIS) è stata eseguita nell'intervallo di frequenza da 0,1 MHz a 10 mHz con un'ampiezza di tensione di 5 mV a circuito aperto. Le misurazioni CV ed EIS sono state eseguite su una stazione di lavoro elettrochimica CHI 660E (Chenhua Instruments Co, Shanghai, Cina). Le celle simmetriche sono state assemblate con Co/C-700 o HEC-700 (8:2 con PVDF in rapporto in peso) come catodo e anodo identici e 50 μL di elettrolita di 1 mol/L LiN(CF3SO2)2, 1% in peso di LiNO3 e 0,2 mol/L Li2S6 in soluzione DOL/DME (1:1 in volume). La spettroscopia di impedenza elettrochimica (EIS) è stata eseguita nell'intervallo di frequenza da 0,1 MHz a 10 mHz con un'ampiezza di tensione di 5 mV a circuito aperto. Le misurazioni CV ed EIS sono state eseguite su una stazione di lavoro elettrochimica CHI 660E (Chenhua Instruments Co, Shanghai, Cina). Le celle simmetriche sono state assemblate con Co/C-700 o HEC-700 (8:2 con PVDF in rapporto in peso) come catodo e anodo identici e 50 μL di elettrolita di 1 mol/L LiN(CF3SO2)2, 1% in peso di LiNO3 e 0,2 mol/L Li2S6 in soluzione DOL/DME (1:1 in volume).
2 Risultati e discussione
La Fig. 1 mostra l'illustrazione schematica della procedura sintetica per il composito di carbonio drogato con cobalto tridimensionale (3D). Quando il citrato di sodio (SC) è stato ricotto in atmosfera inerte, le specie Na+ si sono trasformate in cristalli di Na2CO3 mentre sulla superficie sono comparsi nanofogli di carbonio ultrasottili. Con l'ulteriore aumento della temperatura, i cristalli agiscono come agente attivante e reagiscono con il carbonio rivestito per formare i gusci porosi straticolati. Nel frattempo, gli elementi di cobalto sono stati trasformati in nanoparticelle di Co e incorporati nella struttura di carbonio con la riduzione termica del carbonio.
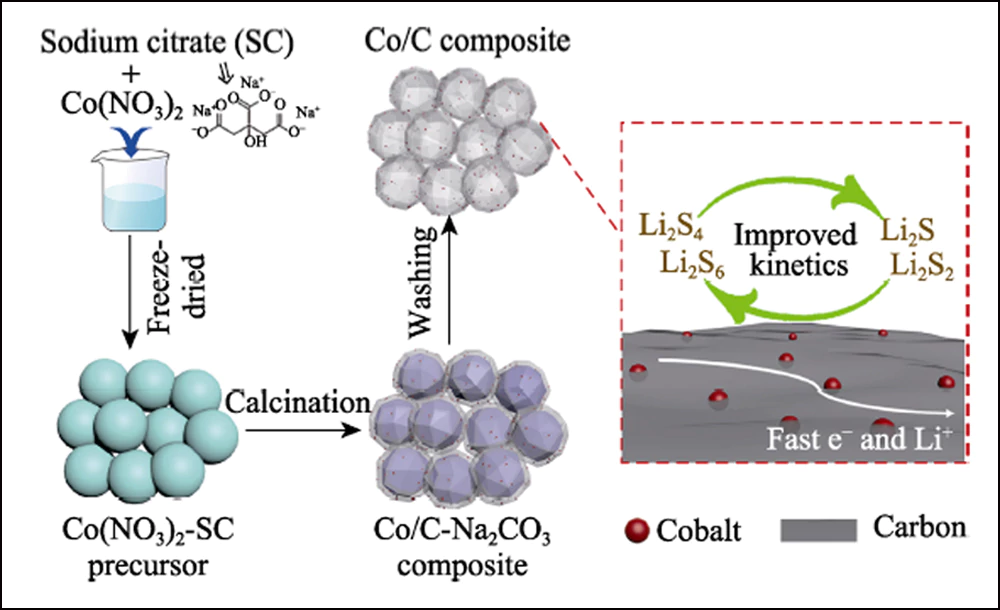
Fig. 1 Illustrazione schematica per le fasi di sintesi del composito Co/C cavo e il suo effetto per l'elettrodo risultante
La composizione e la struttura cristallina di UWC-700 e Co/C-700 sono state caratterizzate da XRD. I principali picchi di diffrazione di UWC-700 (Fig. S1) sono coerenti con Na2CO3 monoclino (PDF#72-0628), mentre altri tre picchi a 2θ=44,2°, 51,5° e 75,9° si adattano bene ai dati cristallini di Co (PDF) #15-0806), che indica la totale decomposizione di SC e la riduzione dell'elemento cobalto. Il pattern XRD di Co/C-700 (Fig. 2(a)) con solo picchi caratteristici del cobalto metallico suggerisce la completa rimozione di Na2CO3. Inoltre, l'evidente ampio picco a circa 2θ=26° rappresenta il piano (002) del carbonio grafitizzato. Nel frattempo, come mostrato negli spettri Raman (Fig. 2 (b)) di Co/C-700, il rapporto di intensità per le due bande evidenti di D (1382 cm-1) e G (1594 cm-1) è 0,866, rispondendo al suo alto grado grafitizzato. Inoltre, il piccolo picco a 680 cm-1 è il caratteristico picco del cobalto. La curva TGA di Co/C-700 è mostrata in Fig. S2(a) per garantire il contenuto di Co. Il prodotto finale (17,83% in peso) dopo il test TGA può essere identificato come Co3O4 (Fig. S2(b)) e il contenuto di Co corrispondente in Co/C-700 è 13,09% in peso secondo il calcolo, che si adatta bene al risultato XPS (Fig. 2 (c)), i rapporti atomici e ponderali di Co sono rispettivamente 3,24at% e 13,66% in peso.
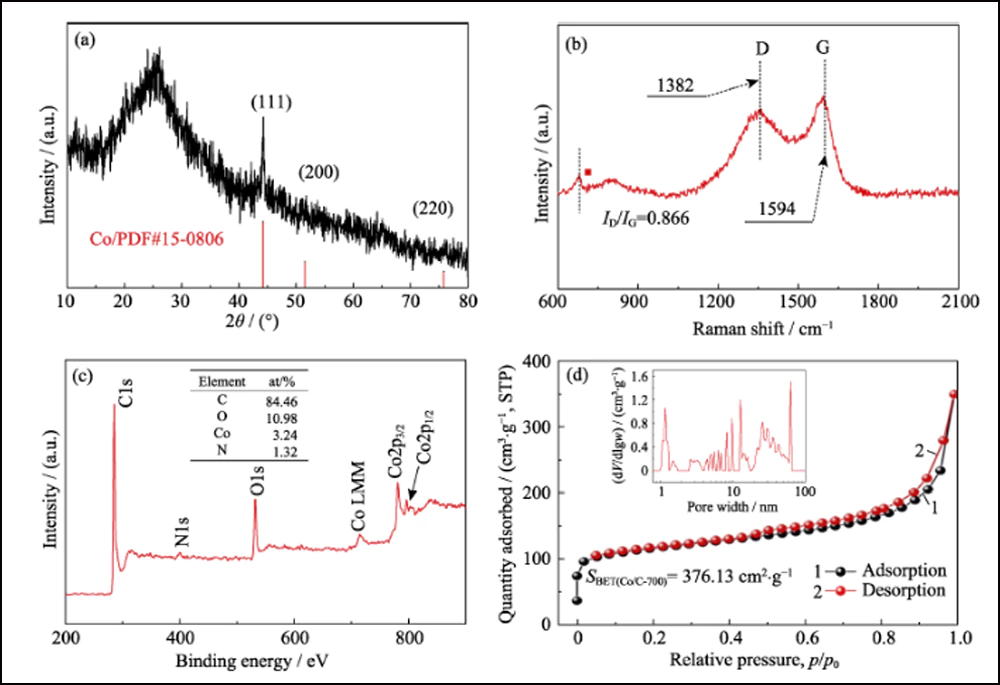
Fig. 2 (a) pattern XRD, (b) spettro Raman, (c) spettro XPS e (d) isoterma di adsorbimento/desorbimento N2 di Co/C-700 con inserto in (d) che mostra la distribuzione delle dimensioni dei pori
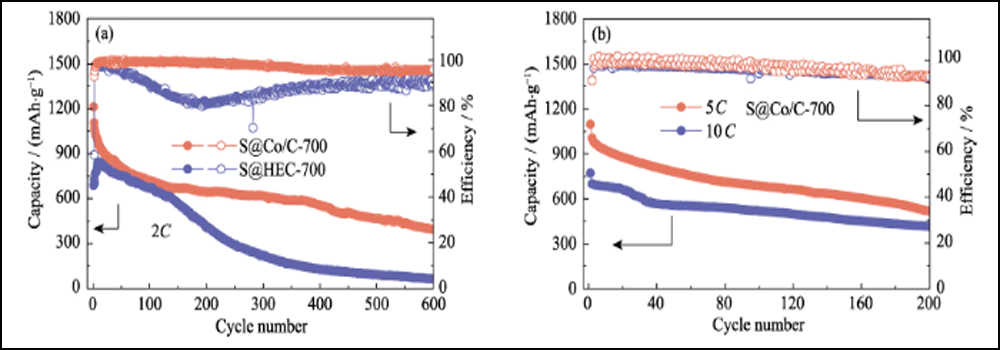
Fig. Modello S1 XRD di UWC-700
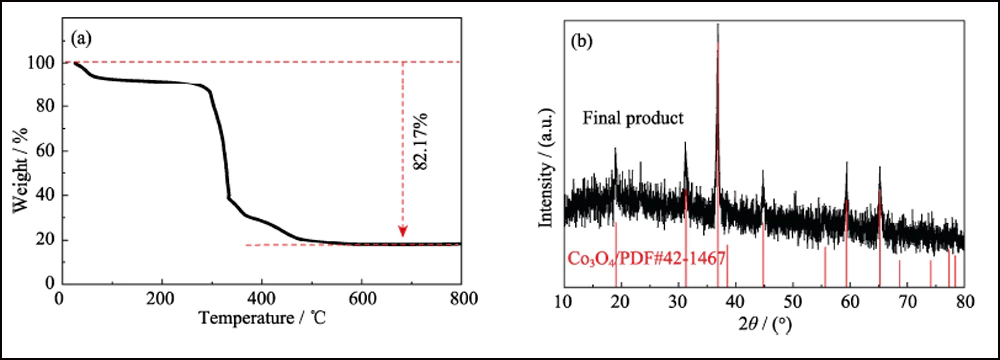
Fig. S2 (a) curva TGA di Co/C-700 in aria e (b) pattern XRD del prodotto finale
La struttura porosa di Co/C è stata caratterizzata dai metodi BET. L'isoterma di adsorbimento-desorbimento N2 (Fig. 2 (d)) mostra un distinto ciclo di isteresi, che rappresenta l'abbondante struttura mesoporosa. Il valore della superficie specifica e il volume dei pori sono stati misurati rispettivamente in 376,13 m2∙g-1 e 0,52 cm3∙g-1. La distribuzione delle dimensioni dei pori (riquadro nella Fig. 2 (d)) determinata dal metodo Barrett-Joyner-Halenda (BJH) mostra una struttura gerarchicamente porosa distinta con un'elevata mesoporosità (62,76%, Tabella S1). Il mesoporo interconnesso e l'elevata area superficiale possono esporre adeguatamente i siti di cobalto per l'adsorbimento e l'ulteriore miglioramento della reazione redox. Inoltre, gli stessi test sono stati eseguiti con gli altri due campioni, UWC-700 e HEC-700 (Fig. S3). La superficie estremamente ridotta (15,09 m2∙g-1) e il volume dei pori (0, 026 cm3∙g-1) di UWC-700 mostrano che la maggior parte dei pori è riempita con i cristalli di Na2CO3. L'area superficiale e il volume dei pori di HEC-700 sono quasi gli stessi di Co/C-700, il che significa la buona conservazione della struttura in carbonio durante le fasi di incisione. Inoltre, il volume del mesoporo in HEC-700 (Tabella S1) è aumentato del 5,4% dopo l'attacco, confermando che le nanoparticelle di Co erano di dimensioni mesoporose.
La morfologia e la struttura di Co/C-700 sono state caratterizzate da SEM (Fig. S4) e TEM (Fig. 3 (a, b)). Le particelle di Co/C-700 mostrano la struttura del guscio di carbonio interconnesso 3D. L'immagine TEM (HRTEM) ad alta risoluzione (Fig. 3 (c)) mostra inoltre che le frange reticolari della nanoparticella con una spaziatura d di 0, 205 nm corrispondono al piano (111) del cobalto metallico. La spaziatura d delle frange storte che avvolgono la nanoparticella (0,35 nm) è in buon accordo con il piano (002) del carbonio grafitico. Le immagini della mappatura EDS (Fig. 3 (d)) mostrano la distribuzione degli elementi Co, C e O, confermando che l'elemento cobalto si disperde uniformemente sui gusci di carbonio.
Tabella S1 BET superficie e distribuzione del volume dei pori di UWC-700, Co/C-700 e HEC-700
|
Campione |
SBET/(m2∙g-1) |
Vtotale/(cm3∙g-1) |
Volume dei pori e/% |
||
|
Micro |
Meso |
Macro |
|||
|
UWC-700 |
15.09 |
0,026 |
1.76 |
98.24 |
0 |
|
Co/C-700 |
376.13 |
0,52 |
28.85 |
62.76 |
8.49 |
|
HEC-700 |
369.53 |
0,54 |
25.47 |
68.17 |
6.36 |

Fig. 3 (a, b) TEM, (c) immagini TEM ad alta risoluzione (HRTEM) e (d) mappature elementari EDS (Co, C e O) di Co/C-700
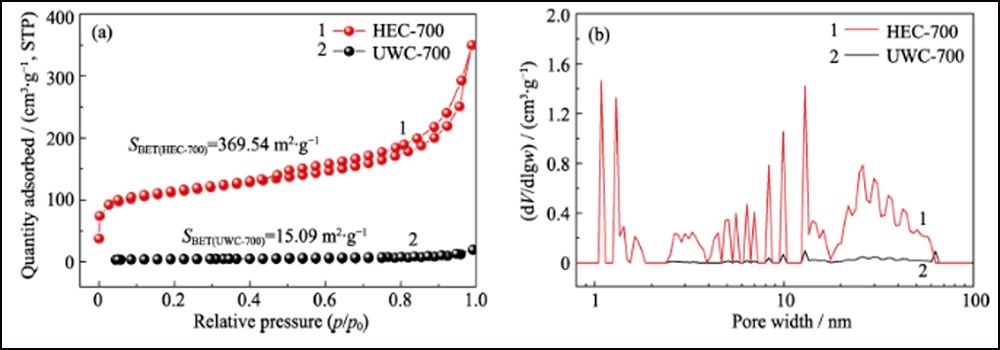
Fig. S3 Isoterme di adsorbimento/desorbimento N2 (a) e distribuzione delle dimensioni dei pori (b) di UWC-700 e HEC-700

Fig. Immagine S4 SEM di Co/C-700
Per confermare ulteriormente l'effetto elettrochimico delle Conanoparticles nelle batterie Li-S, è stato impiegato HEC-700 come campione di controllo. Il modello XRD, l'immagine SEM (Fig. S5) e i dati BET mostrano che HEC-700 possiede quasi la stessa struttura di Co/C-700, ad eccezione dell'esistenza dell'elemento Co. Gli elettrodi S@Co/C-700 e S@HEC-700 sono stati preparati come catodi per batterie Li-S. Come mostrato in Fig. S6, la principale perdita di peso tra la temperatura ambiente e 450 ℃ è attribuita alla sublimazione dello zolfo, corrispondente al contenuto di zolfo del 70,99% in peso e del 68,42% in peso in S@Co/C-700 e S@HEC - 700, rispettivamente.
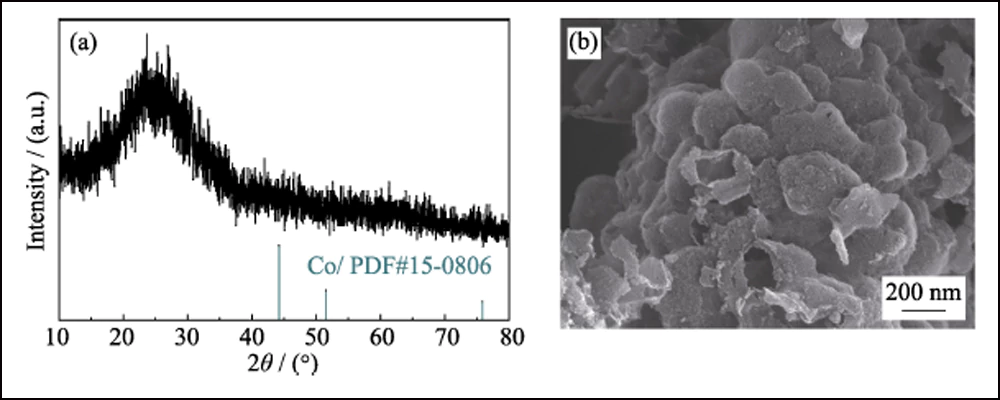
Fig. Modello XRD S5 (a) e immagine SEM (b) di HEC-700
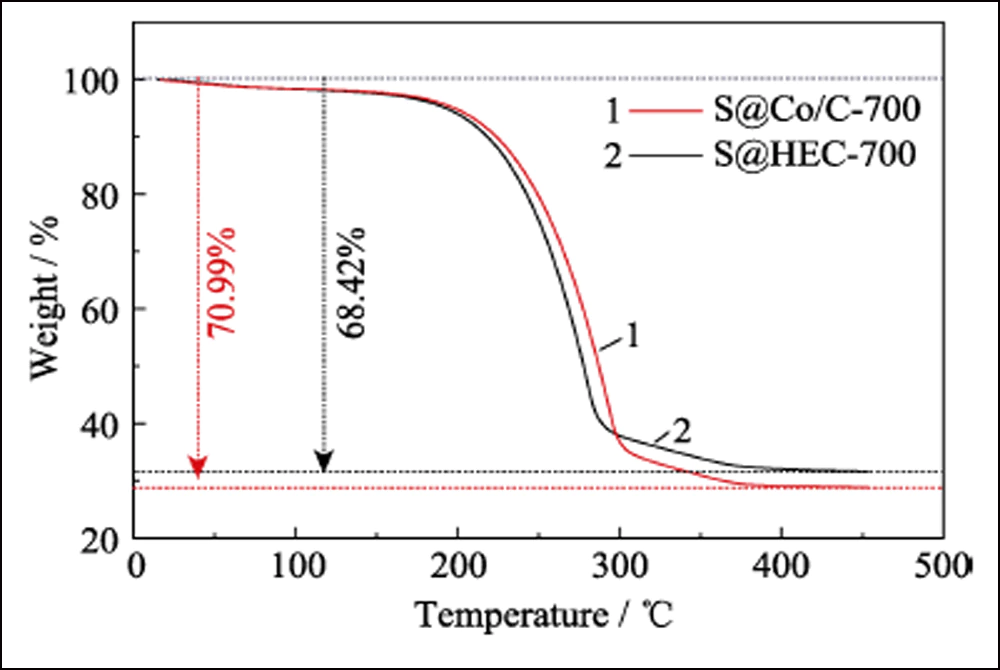
Fig. S6 Curve TGA di S@Co/C-700 e S@HEC-700 in atmosfera di N2
La composizione superficiale di S@Co/C-700 è stata studiata mediante XPS. Lo spettro di rilevamento (Fig. S7) mostra la presenza di elementi S, C, N, O e Co sulla superficie del composito. La piccola N è dal precursore di Co(NO3)2. Il rapporto estremamente basso di zolfo (7,83at%) indica che il cristallo di zolfo si è infiltrato con successo nella struttura porosa. Lo spettro ad alta risoluzione di S2p (Fig. 4 (a)) mostra quattro picchi principali. I picchi a 164 e 165,2 eV corrispondono rispettivamente a S2p3/2 e S2p1/2. I picchi situati a 169 e 170,1 eV sono attribuiti rispettivamente a tiosolfato e S-Co. Lo spettro C1s è presentato in Fig. 4 (b). I picchi a 284,8, 285,6 e 288,8 eV corrispondono a legami CC, CO e O=CO, quasi gli stessi dello spettro C1s di Co/C-700 (Fig. S8(a)). E lo spettro di O1s (Fig. 4 (c)) mostra O=C, OC e O= CO rispettivamente a 531,6, 532,4 e 533,4 eV. Se confrontati con Co/C-700 (Fig. S8 (b)), tutti questi picchi si spostano di oltre 0,5 eV e verificano ulteriormente l'interazione tra i gruppi funzionali di zolfo e ossigeno. Inoltre, lo spettro di Co2p in Fig. 4 (d) mostra due picchi principali di Co2p3/2 e Co2p1/2 a 780,3 e 797,9 eV, che rappresentano per il metallo di cobalto. Diversamente dalle curve di Co/C-700 (Fig. S8(c)), compaiono due picchi extra a 783,7 e 800,4 eV in S@Co/C-700 che suggeriscono la forte interazione tra zolfo e cobalto. Il test di adsorbimento statico è stato impiegato per studiare l'interazione tra LiPS e Co/C-700 o HEC-700 in modo più intuitivo. E la fotografia rivela la soluzione incolore di Co/C-700 e il colore quasi invariato di HEC-700 (Fig. S9).
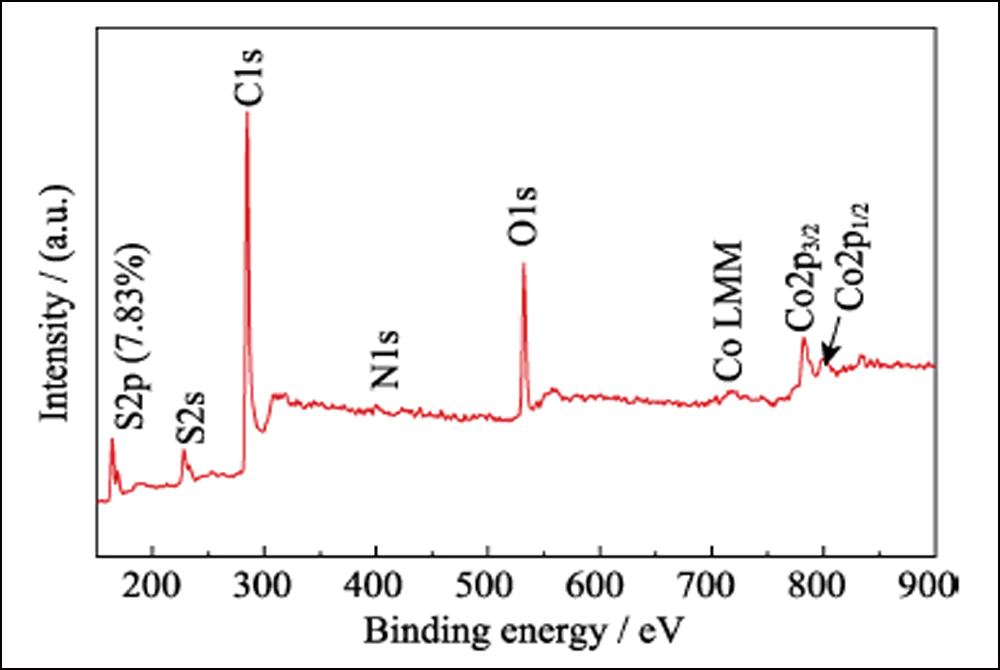
Fig. Spettro S7 XPS del composito S@Co/C-700
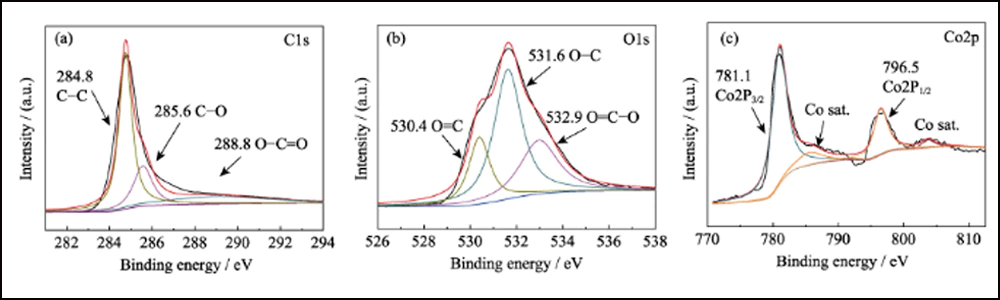
Fig. S8 Spettri XPS ad alta risoluzione di Co/C-700(a) C1; (b) O1; (c) Co2p
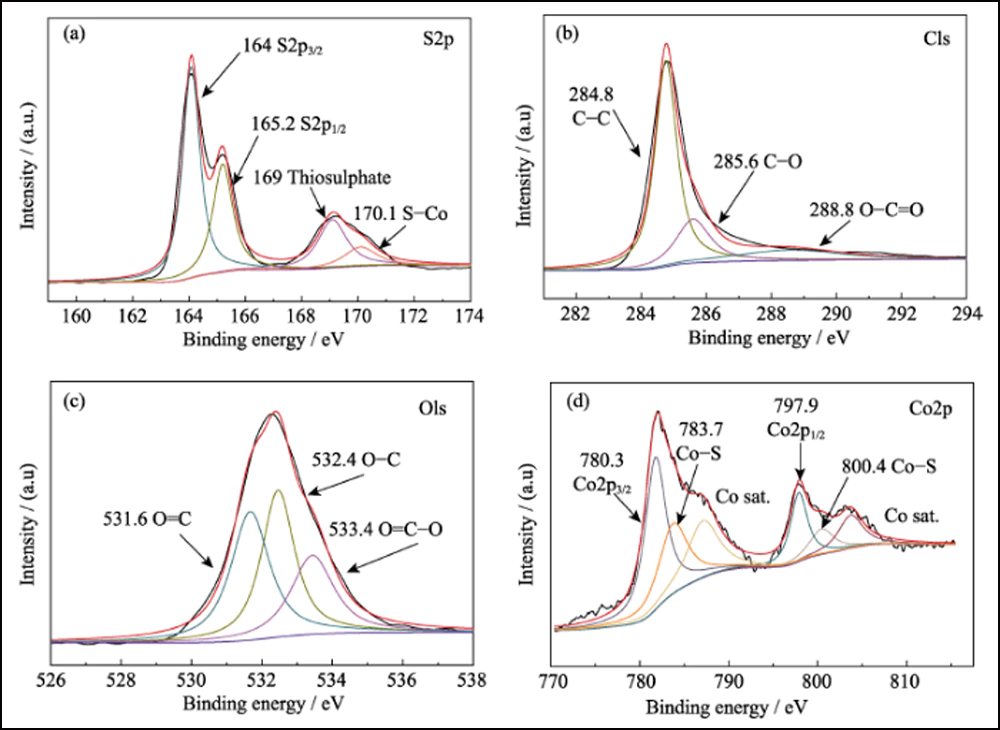
Fig. 4 Spettri XPS ad alta risoluzione per compositi S@Co/C-700
(a) S2p; (b) C1; (c) O1; (d) Co2p

Fig. S9 Fotografia del test di adsorbimento statico di HEC-700 e Co/C-700 dopo 1 h
Oltre all'efficace adsorbimento e alla forte interazione, le nanoparticelle di cobalto droganti possono migliorare efficacemente la cinetica della reazione di conversione tra S8 e Li2S. La voltammetria ciclica (CV) delle celle simmetriche con elettrodi Co/C-700 e HEC-700 è stata utilizzata per confermare l'effetto delle nanoparticelle di cobalto. Le curve CV in Fig. 5 (a) rivelano chiaramente otto picchi redox con grande sovrapposizione (Fig. S10 (a)). La separazione e la stabilità dei picchi redox indicano la migliore reversibilità e cinetica della reazione di conversione. Inoltre, la curva della prima scansione a -1 V rivela tre picchi che rappresentano la riduzione graduale da Li2S6 originale a Li2S insolubile sull'elettrodo di lavoro e l'ossidazione di Li2S6 sul controelettrodo. I quattro picchi a -0,112, 0,093, 0,326 e 0. 401 V rappresentano l'ossidazione graduale da Li2S all'elemento zolfo sull'elettrodo di lavoro. Pertanto, il picco a 0,112 V corrisponde alla riduzione da S8 a Li2S6. Inoltre, i picchi con una buona sostenibilità con velocità di scansione più elevate (Fig. S10 (b)) indicano anche l'efficiente processo elettrochimico basato sugli elettrodi Co/C-700. Al contrario, il controllo sperimentale degli elettrodi HEC-700 mostra solo due coppie di ampi picchi (Fig. 5 (b)) con la deriva ciclica (Fig. S10 (c)) e i picchi poco appariscenti a -0,264/0,264 V diventano invisibile a tassi più elevati (Fig. S10 (d)), indicando la cinetica lenta e la conversione incompleta della reazione dei polisolfuri senza l'esistenza di nanoparticelle di Co. i picchi con una buona sostenibilità con velocità di scansione più elevate (Fig. S10 (b)) indicano anche l'efficiente processo elettrochimico basato sugli elettrodi Co/C-700. Al contrario, il controllo sperimentale degli elettrodi HEC-700 mostra solo due coppie di ampi picchi (Fig. 5 (b)) con la deriva ciclica (Fig. S10 (c)) e i picchi poco appariscenti a -0,264/0,264 V diventano invisibile a tassi più elevati (Fig. S10 (d)), indicando la cinetica lenta e la conversione incompleta della reazione dei polisolfuri senza l'esistenza di nanoparticelle di Co. i picchi con una buona sostenibilità con velocità di scansione più elevate (Fig. S10 (b)) indicano anche l'efficiente processo elettrochimico basato sugli elettrodi Co/C-700. Al contrario, il controllo sperimentale degli elettrodi HEC-700 mostra solo due coppie di ampi picchi (Fig. 5 (b)) con la deriva ciclica (Fig. S10 (c)) e i picchi poco appariscenti a -0,264/0,264 V diventano invisibile a tassi più elevati (Fig. S10 (d)), indicando la cinetica lenta e la conversione incompleta della reazione dei polisolfuri senza l'esistenza di nanoparticelle di Co.
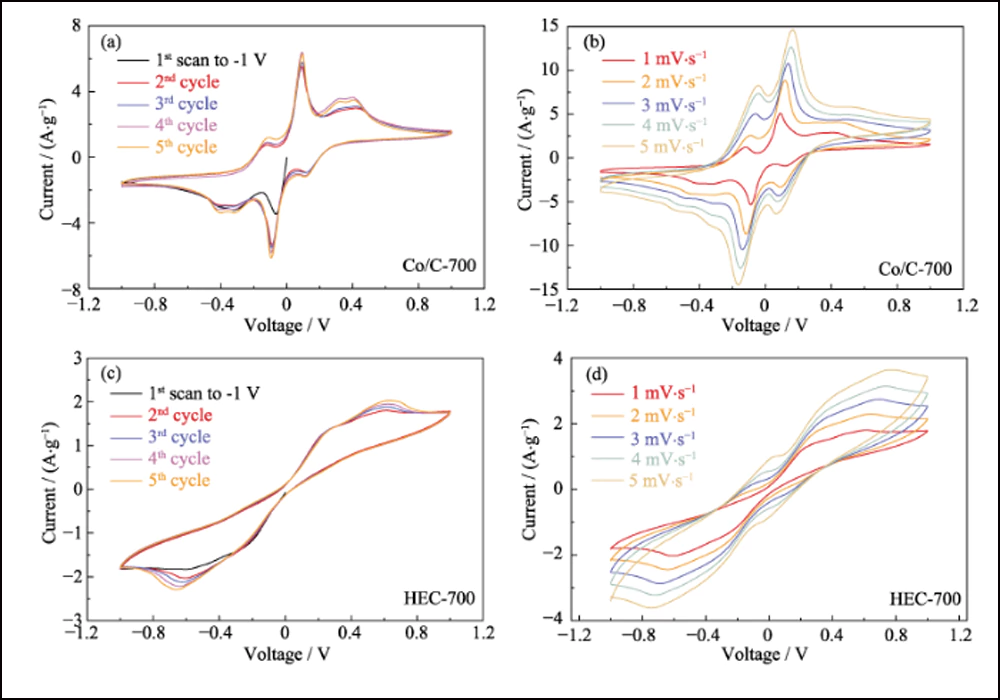
Fig. S10 Curve CV multiciclo di celle simmetriche basate su Co/C-700 a 1 mV∙s-1 (a) e tassi aumentati (b) e curve CV multiciclo di HEC-700 a 1 mV∙s- 1 (c) e aliquote maggiorate (d)
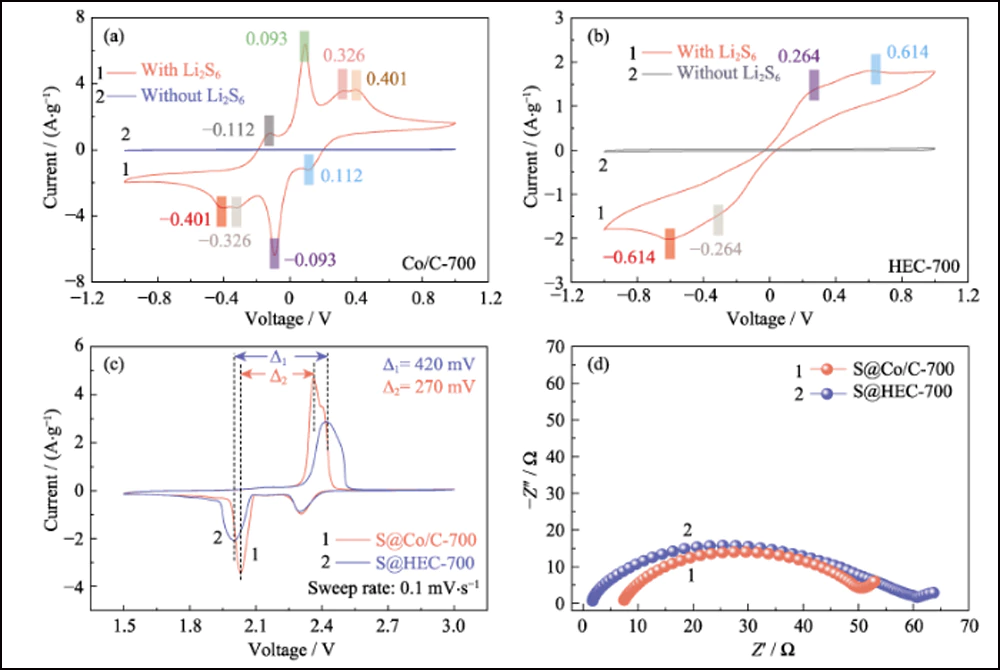
Fig. 5 Curve CV di (a) celle simmetriche basate su Co/C-700 e (b) HEC-700 con e senza 0,2 mol∙L-1 Li2S6 a 1 mV∙s-1; (c) curve CV e (d) grafici EIS degli elettrodi S@Co/C-700 e S@HEC-700
Per confermare ulteriormente la cinetica elettrochimica potenziata in presenza di nanoparticelle di cobalto, i test CV degli elettrodi S@Co/C-700 e S@HEC-700 (Fig. 5(c)) sono stati misurati con una velocità di scansione di 0,1 mV∙ s-1. Per il processo di riduzione catodica di S@Co/C-700, due picchi reversibili a 2,306 e 2,031 V sono associati rispettivamente alla trasformazione da zolfo a LiPS solubili e all'ulteriore riduzione a Li2S2/Li2S insolubile. In confronto, l'ultimo picco di riduzione di S@HEC-700 mostra uno spostamento negativo significativo. Suggerisce la cinetica di reazione più lenta, che può aumentare il tempo di detenzione dei LiPS e aggravare l'effetto di spola. Per il processo anodico, il processo di ossidazione di S@Co/C-700 rivela un picco discreto a 2,397 V e un picco maggiore a 2,361 V, corrispondente all'ossidazione da Li2S2/Li2S a LiPSs e successivamente a zolfo, rispettivamente. La separazione dei picchi di ossidazione mostra la cinetica migliorata della prima reazione. Inoltre, l'intervallo tra il secondo picco di riduzione e il picco di ossidazione maggiore di S@Co/C-700 (270 mV, Fig. 5(c)) è significativamente inferiore a quello di S@HEC-700 (420 mV), indicando il sovrapotenziale di polarizzazione ridotto e la cinetica migliorata della reazione redox con l'esistenza del cobalto. Le curve EIS (Fig. 5(d)) mostrano una minore resistenza al trasferimento di carica (la dimensione del semicerchio ad alta frequenza) dell'elettrodo S@Co/C-700 (43,1 Ω) rispetto a quella di S@HEC-700 (58,7 Ω ), che rivela anche la maggiore cinetica di reazione del cobalto. 5 (c)) è significativamente più piccolo di quello di S @ HEC-700 (420 mV), indicando il sovrapotenziale di polarizzazione ridotto e la cinetica migliorata della reazione redox con l'esistenza di cobalto. Le curve EIS (Fig. 5(d)) mostrano una minore resistenza al trasferimento di carica (la dimensione del semicerchio ad alta frequenza) dell'elettrodo S@Co/C-700 (43,1 Ω) rispetto a quella di S@HEC-700 (58,7 Ω ), che rivela anche la maggiore cinetica di reazione del cobalto. 5 (c)) è significativamente più piccolo di quello di S @ HEC-700 (420 mV), indicando il sovrapotenziale di polarizzazione ridotto e la cinetica migliorata della reazione redox con l'esistenza di cobalto. Le curve EIS (Fig. 5(d)) mostrano una minore resistenza al trasferimento di carica (la dimensione del semicerchio ad alta frequenza) dell'elettrodo S@Co/C-700 (43,1 Ω) rispetto a quella di S@HEC-700 (58,7 Ω ), che rivela anche la maggiore cinetica di reazione del cobalto.
La Fig. 6 confronta le prestazioni elettrochimiche dei catodi S@Co/C-700 e S@HEC-700. Le capacità di velocità di S@Co/C-700 (Fig. 6(a)) mostrano una capacità di scarica iniziale molto più elevata (1280 mAh∙g-1) rispetto a S@HEC-700 (847 mAh∙g-1) al velocità di corrente di 0,5°C (1°C = 1672 mAh∙g-1). A velocità di ciclo più elevate di 1°C, 2°C, 5°C e 10°C, le capacità di scarica del catodo S@Co/C-700 raggiungono 1058, 948, 867 e 797 mAh∙g-1 e recuperano ulteriormente a 968 mAh∙g-1 a 1C (95 % del 10° ciclo). E i profili di tensione di carica-scarica galvanostatici a velocità diverse mostrano che l'elettrodo S@Co/C-700 esercita un plateau di scarica più piccolo e molto più lungo anche a 10°C (Fig. S11). Le stabilità del ciclo dei due catodi a velocità 1C sono confrontate in Fig. 6 (b). Il catodo S@Co/C-700 mostra un'elevata capacità iniziale di 1244 mAh∙g-1, e mantiene 770 mAh∙g-1 dopo 200 cicli con un'elevata efficienza Coulomb (superiore al 96%), rivelando una capacità molto più elevata e una migliore stabilità rispetto all'S@HEC-700. Le prestazioni ciclistiche a lungo termine a 2C mostrate in Fig. S12 (a). Dopo 600 cicli, il catodo S@Co/C-700 ha mantenuto una capacità di scarica di 401,7 mAh∙g-1 (65,3 mAh∙g-1 per S@HEC-700). Le velocità estremamente elevate a 5°C e 10°C vengono ulteriormente valutate per il catodo S@Co/C-700 (Fig. S12(b)). Mostra elevate capacità di scarica iniziale (1098 e 772 mAh∙g-1 rispettivamente a 5°C e 10°C) senza alcuna fase di attivazione e prestazioni cicliche stabili (518 e 416 mAh∙g-1 rispettivamente a 5°C e 10°C) per più di 200 cicli. La stabilità del ciclo più eccellente e le prestazioni di velocità dell'elettrodo S@Co/C-700 sono attribuite ai vantaggi delle nanoparticelle di cobalto.
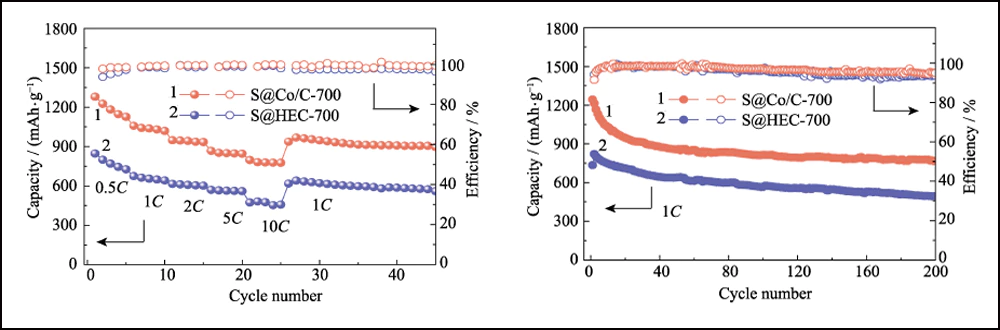
Fig. 6 (a) Capacità di frequenza a varie velocità da 0,5°C a 10°C e (b) stabilità del ciclo a 1°C per elettrodi S@Co/C-700 e S@HEC-700
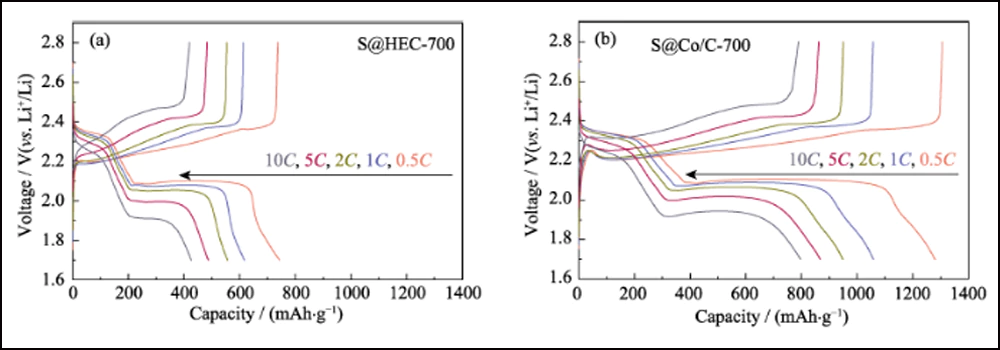
Fig. S11 Profili di tensione degli elettrodi S@HEC-700 (a) e S@Co/C-700 (b) a varie velocità da 0,5°C a 10°C
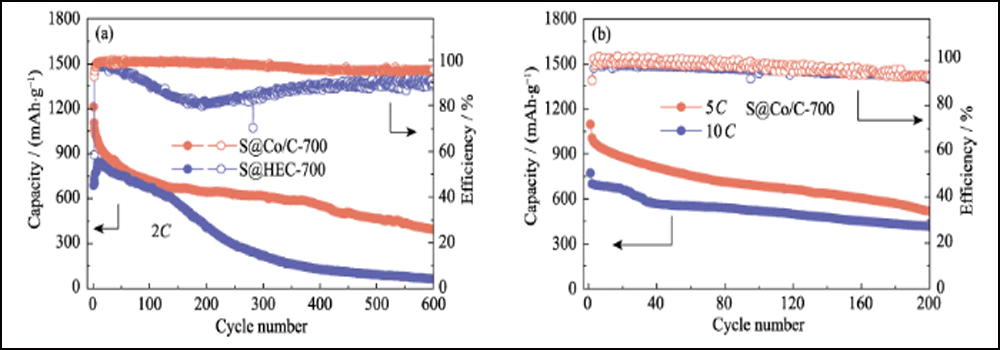
Fig. S12 (a) Stabilità ciclica degli elettrodi S@Co/C-700 e S@HEC-700 a 2C; (b) Prestazioni ciclistiche di S@Co/C-700 a 5°C e 10°C
3 Conclusione
In sintesi, progettiamo una sintesi su larga scala di compositi Co/C-700 come materiale ospite per supportare lo zolfo per le batterie Li-S. Combinando con i risultati di CV ed EIS, concludiamo che le nanoparticelle di Co incorporate riducono il sovrapotenziale e promuovono la cinetica di conversione dei LiPS. Inoltre, l'XPS e il test di adsorbimento statico mostrano la forte interazione tra LiPS e Co drogato. Con la cooperazione di Co e l'esclusiva struttura porosa cava, i catodi S@Co/C-700 ottenuti mostrano un'elevata capacità specifica di 1280 mAh∙g -1 a 0,5°C e prestazioni stabili a ciclo lungo da 1°C a 10°C. Questo lavoro dimostra la fattibilità di batterie Li-S ad alta densità di energia con il drogante del metallo di cobalto per requisiti ad alta velocità.
Materiali di supporto
Struttura di carbonio cavo drogata con cobalto come ospite di zolfo per il catodo della batteria al litio zolfo
JIN Gaoyao, HE Haichuan, WU Jie, ZHANG Mengyuan, LI Yajuan, LIU Younian
Hunan Provincial Key Laboratory of Micro & Nano Materials Interface Science, College of Chemistry and Chemical Engineering, Central South University, Changsha 410083, China
Materials characterization
The crystalline structures of the as-synthesized samples were characterized by X-ray power diffraction (XRD, Dmax/2550VB, Rigaku, Japan) with Cu Kα radiation. The surface morphology and microstructure were obtained by a scanning electron microscopy (SEM, FEI Verios 460). Transmission electron microscopy (TEM, JEM-2100F) equipped with an X-ray energy dispersive spectrometer (EDS) was used to collect transmission and high-resolution images of the Co/C-700. The Co content in Co/C-700 and S content in S@Co/C- 700 or S@HEC-700 were determined by thermogravimetric analyzer (TGA, Q600, USA) in air or N2, respectively, with a heating rate of 10 ℃∙min-1. Raman spectroscopy was performed using a reflex Raman system (Renishaw in Via Raman microscope, UK) equipped with a microscope under 532 nm laser radiation at 50 mW. X-ray photoelectron spectrometer (XPS) analysis was performed at an ESCALAB 250XI X-ray photoelectron spectrometer (Thermo Fisher Scientific, USA). The specific surface area and pore size distribution of samples were determined by nitrogen adsorption- desorption analysis.
Static adsorption of polysulfides
Typically, 0.003 mol/L Li2S6 solution was obtained by reacting stoichiometric Li2S and S in 1,2-dimethoxyethane(DME) and 1,3-dioxolane(DOL) (1 : 1 in volume) at 60 ℃ for 24 h. Then, 10 mg Co/C-700 or HEC-700 was added into 3 mL of the lithium polysulfide solution. The photograph was taken after the sample stood for 1 h.